Lernziel
- Erkennen der Beziehungen zwischen Konstitutionsisomeren (Strukturisomeren), Konformationsisomeren und geometrischen Isomeren
Isomere
Isomere haben immer die gleiche chemische Formel. Wenn die chemischen Formeln unterschiedlich sind, dann handelt es sich um völlig unterschiedliche Verbindungen. Aus den chemischen Formeln können beim Vergleich von Verbindungen wichtige Informationen gewonnen werden.
Strukturisomere (Konstitutionsisomere) haben die gleiche Summenformel, aber eine unterschiedliche Bindungsanordnung der Atome. Stereoisomere haben identische Summenformeln und Anordnungen der Atome. Sie unterscheiden sich nur durch die räumliche Anordnung der Gruppen im Molekül. In der organischen Chemie gibt es mehrere Arten von Stereoisomeren: Enantiomere, Diasteriomere, geometrische Isomere und Konformere. Diese Stereoisomere werden in mehreren Kapiteln vorgestellt und erklärt.
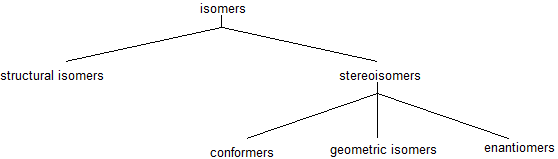
Strukturelle (konstitutionelle) Isomere
Da Kohlenstoff vier Bindungen bildet, kann es mehrere Möglichkeiten geben, Moleküle zu bilden, die der Oktettregel folgen. Selbst bei nur vier Kohlenstoffatomen gibt es zwei mögliche Strukturen für das Kohlenstoffgerüst. Die Kohlenstoffatome können zu einer Vier-Kohlenstoff-Kette verbunden sein (Butan) oder es kann eine Ein-Kohlenstoff-Verzweigung von einer Drei-Kohlenstoff-Kette geben (2-Methylpropan). Butan und 2-Methylpropan sind strukturelle Isomere, da sie beide die chemische Formel C4H10 haben.

Identisch vs. Konformer
Die Rotation um Einzelbindungen erzeugt dynamische Moleküle. Beim Zeichnen und Diskutieren von Molekülen ist es wichtig, sich bewusst zu machen, dass unsere Zeichnungen statisch sind, während die Moleküle selbst rotieren. Obwohl es im Ethan-Molekül sieben Sigma-Bindungen gibt, führt die Rotation um die sechs Kohlenstoff-Wasserstoff-Bindungen zu keiner Veränderung der Form des Moleküls, da die Wasserstoffatome im Wesentlichen kugelförmig sind. Die Drehung um die Kohlenstoff-Kohlenstoff-Bindung führt jedoch zu vielen verschiedenen möglichen Molekülkonformationen. Konformere sind das einfachste Beispiel für Stereoisomerie.
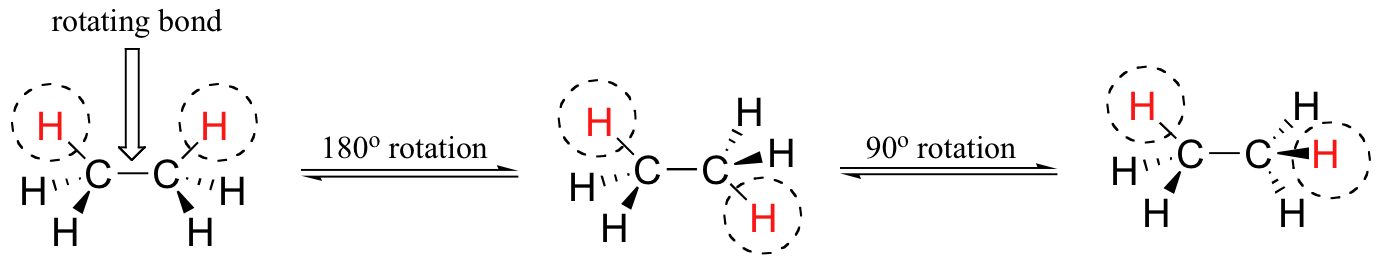
Identische Verbindungen sind die gleiche Verbindung, die mit ALLEN Atomen in der gleichen räumlichen Orientierung dargestellt wird.
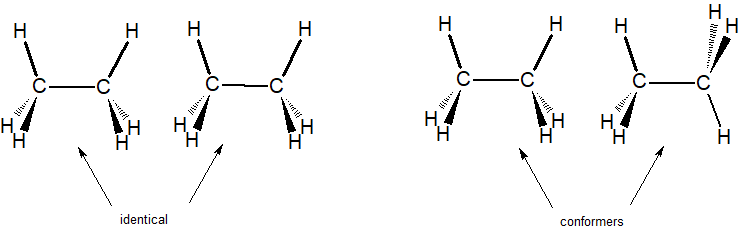
Konformere sind die gleiche Verbindung, die mit unterschiedlichen Rotationen um Einzelbindungen dargestellt wird.
Im folgenden Beispiel können wir zwei identische Strukturen für Ethan mit zwei Konformeren von Ethan vergleichen.
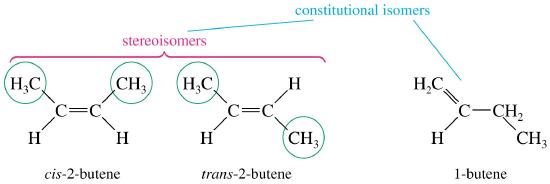
Geometrische Isomere – ein Beispiel für Stereoisomerie
Die Starrheit der pi-Bindungen in Doppelbindungen kann geometrische Isomerie erzeugen. Ohne Rotation sind zwei verschiedene Orientierungen an der Kohlenstoff-Kohlenstoff-Doppelbindung (C=C) möglich. Die Starrheit der Doppelbindung schafft eine Bezugslinie für die räumliche Orientierung. Die Vorsilben cis und trans werden zur Unterscheidung der geometrischen Isomere verwendet. Beim cis-Stereoisomer befinden sich beide Nicht-Wasserstoffatome auf der gleichen Seite der Doppelbindung. Das trans-Stereoisomer hingegen hat die Nicht-Wasserstoffatome auf der anderen Seite der Doppelbindung. Auf die gleiche Weise überqueren wir den Ozean bei einer transatlantischen Reise. Dieser kleine Unterschied mag unbedeutend erscheinen, aber geometrische Isomere sind unterschiedliche chemische Verbindungen mit unterschiedlichen physikalischen Eigenschaften, wie das Beispiel unten zeigt.

Fürs Erste ist es wichtig, beim Vergleich von Verbindungen zwischen strukturellen und räumlichen Unterschieden zu unterscheiden. In der Zukunft werden wir die Isomerie genauer betrachten.
Beispiel
Lassen Sie uns die untenstehenden Bindungsstrukturen betrachten und die Beziehungen zwischen den folgenden Paaren von Verbindungen bestimmen: identisch, konform, strukturelle Isomere, geometrische Isomere oder völlig unterschiedliche Verbindungen.
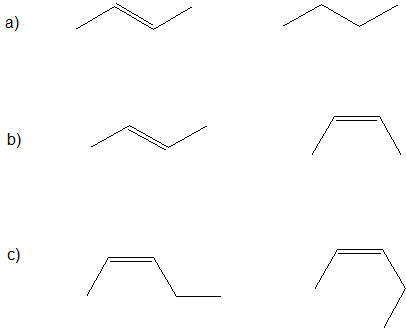
Der erste wichtige Schritt (der oft übersprungen wird) ist die Bestimmung der chemischen Formeln der einzelnen Verbindungen. Wenn die chemischen Formeln unterschiedlich sind, dann sind die Verbindungen völlig unterschiedlich und es gibt KEINE isomere Beziehung. Wenn die chemischen Formeln gleich sind, müssen wir den Unterschied zwischen den Verbindungen identifizieren, um ihre Verwandtschaft zu bestimmen. Wenn es strukturelle Unterschiede in den Bindungsmustern gibt, dann sind die Verbindungen konstitutionell (strukturelle Isomere). Wenn die Verbindungen die gleichen strukturellen Verbindungen haben, aber die räumlichen Ausrichtungen unterschiedlich sind, dann sind die Verbindungen Stereoisomere. Für den Moment sind die möglichen Stereoisomere Konformere, die dieselbe Verbindung mit unterschiedlichen Kohlenstoff-Kohlenstoff-Einfachbindungsrotationen zeigen, oder geometrische Isomere von Verbindungen mit unterschiedlichen Orientierungen an den Kohlenstoff-Kohlenstoff-Doppelbindungen.
Wenn wir die obige Logik auf unser Beispiel anwenden, stellen wir Folgendes fest.
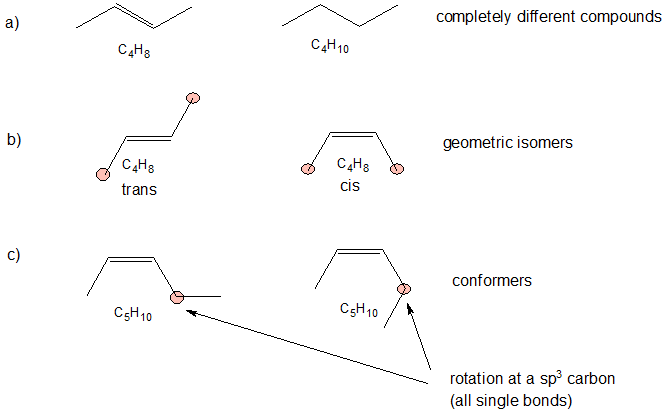
Übung
1. In welchem Verhältnis stehen die folgenden Verbindungspaare zueinander: identisch, konform, Strukturisomere, geometrische Isomere oder völlig unterschiedliche Verbindungen?
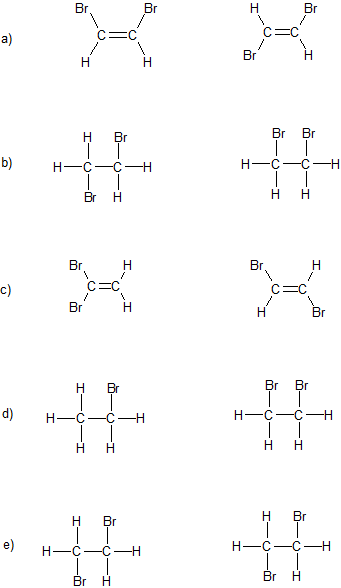
Antwort
a) geometrische Isomere
b) Konformere
c) Strukturisomere
d) völlig unterschiedliche Verbindungen
e) identisch