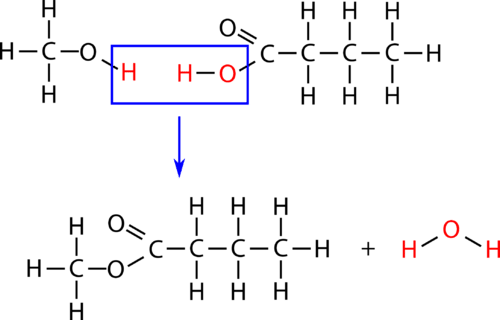
Veresterung
Eine Veresterung ist eine Kondensationsreaktion, bei der ein Ester aus einem Alkohol und einer Carbonsäure gebildet wird. Die Veresterung ist eine Unterkategorie der Kondensationsreaktionen, da bei der Reaktion ein Wassermolekül entsteht. Katalysiert wird die Reaktion durch eine starke Säure, meist Schwefelsäure. Wenn die Carbonsäure Butansäure mit einem Überschuss an Methanol und ein paar Tropfen Schwefelsäure erhitzt wird, entsteht der Ester Methylbutanoat. Methylbutanoat hat den Geruch von Ananas. Die Reaktion ist unten sowohl mit Molekül- als auch Strukturformeln dargestellt.
Die Veresterungsreaktion ist reversibel. Wenn ein Ester in Gegenwart einer starken Base wie Natriumhydroxid erhitzt wird, spaltet sich der Ester. Die Produkte sind ein Alkohol und die konjugierte Base der Carbonsäure als Salz.
Das Natriumhydroxid wirkt nicht als Katalysator, sondern wird bei der Reaktion verbraucht.
Die Verseifung beschreibt die alkalische Hydrolysereaktion eines Esters. Ursprünglich beschrieb der Begriff Verseifung die Hydrolyse von langkettigen Estern, den sogenannten Fettsäureestern, zu Seifenmolekülen, die die Salze der Fettsäuren sind. Ein solches Seifenmolekül ist Natriumstearat, das bei der Hydrolyse von Ethylstearat entsteht.