Originalherausgeber – Bruce Tan als Teil des Projekts „Pathophysiologie komplexer Patientenprobleme“ der Bellarmine University.
Top Contributors – Bruce Tan, Morgan Yoder, Hannah McCabe, Elaine Lonnemann und Wendy Walker
Definition/Beschreibung
Heterotopische Ossifikation (HO) bezieht sich auf die Bildung von lamellarem Knochen innerhalb von Weichteilstrukturen, wo kein Knochen existieren sollte. Die Entstehung von HO ist extraartikulär und findet außerhalb der Gelenkkapsel statt. Der neue Knochen betrifft im Allgemeinen nicht das Periost. Der HO kann auch an der Kortikalis des angrenzenden Knochens ansetzen, wobei es zu einer Unterbrechung der Kortikalis kommen kann. Dieser Prozess kann in Strukturen wie der Haut, dem subkutanen Gewebe, dem Skelettmuskel und dem an den Knochen angrenzenden fibrösen Gewebe auftreten. In selteneren Formen wurde HO in den Wänden von Blutgefäßen und intra-abdominalen Stellen wie dem Mesenterium beschrieben. Der primäre Risikofaktor für HO ist ein auslösendes Trauma. Außerdem hat sich gezeigt, dass Entzündungen eine Rolle bei der Bildung von HO spielen, da Osteoprogenitorzellen in dieser Umgebung zur Proliferation angeregt werden. Zusätzliche Faktoren werden im Abschnitt Ätiologie näher beschrieben. Obwohl HO an jeder Stelle gefunden werden kann, ist sie am häufigsten in den großen Gelenken wie Hüfte, Ellenbogen, Schulter und Knie zu finden.
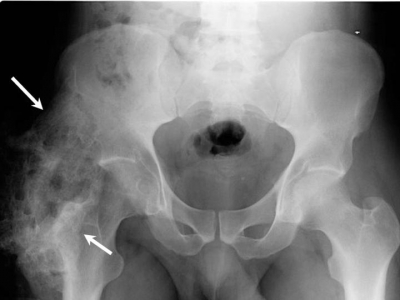
HO wurde erstmals 1692 von Patin beschrieben, als er mit Kindern arbeitete, bei denen eine Myositis ossificans progressiva diagnostiziert wurde. Im Jahr 1918 beschrieb Dejerine & Ceillier die anatomischen, klinischen und histologischen Merkmale der ektopen Knochenbildung bei Soldaten, die im Ersten Weltkrieg Wirbelsäulenverletzungen erlitten hatten.
Nach der Arbeit von Dejerine & Ceillier beschrieb Marshall Urist die osteoinduzierenden Eigenschaften des knochenmorphogenen Proteins in ektopen Bereichen wie dem Muskel. Dies wurde und wird immer noch als eine „bahnbrechende Entdeckung“ in der orthopädischen Forschung angesehen. Zwei der ursprünglichen Forschungsartikel von Urist finden Sie unten:
- Knochen: Bildung durch Autoinduktion
- Bone Morphogenic Protein
Etiologie/Ursachen
Die genaue Pathophysiologie der HO ist unbekannt. An der Umwandlung primitiver mesenchymaler Zellen des Bindegewebes in osteoblastisches Gewebe und Osteoid sind vielfältige und schlecht verstandene Auslöser beteiligt. Zu diesen Auslösern gehören genetische, posttraumatische, neurogene, postoperative und reaktive Läsionen der Hände und Füße.

Genetische Formen umfassen zwei Typen: Fibrodysplasia Ossificans Progressiva (FOP) und Progressive Osseous Heteroplasia(POH). Diese Typen werden als massive Ablagerungen von heterotopem Knochen um mehrere Gelenke herum beschrieben, ohne dass ein auslösendes Ereignis (z. B. ein Trauma) vorliegt. Dies ist die schwerste Form der HO, die sich im Laufe des Lebens fortschreitend bildet und die Gesundheit, Lebenserwartung und Lebensqualität stark beeinträchtigt.
Die posttraumatische HO beginnt mit einer Spindelzellproliferation innerhalb der ersten Woche nach dem traumatischen Ereignis. Innerhalb von 1-2 Wochen entwickelt sich primitives Osteoid. Nach der zweiten Woche sind primitiver Knorpel und gewebter Knochen zu sehen. Trabekelknochen bildet sich 2-5 Wochen nach dem Trauma. Amorphes Calciumphosphat wird mit fortschreitender Mineralisierung allmählich durch Hydroxylapatitkristalle ersetzt. Nach etwa 6 Monaten zeigt sich echter Knochen im Bindegewebe zwischen den Muskelebenen.
Neurogene heterotope Ossifikation tritt nach Sichelzellanämie, Hämophilie, Tetanus, Poliomyelitis, Multipler Sklerose und toxischer epidermaler Nekrolyse auf. Neurogene HO entwickelt sich nur an Stellen, die distal der Ebene der Rückenmarksverletzung liegen. Die von HO betroffenen Areale befinden sich fast immer auf der betroffenen Seite der Hirnverletzung oder des Schlaganfalls.
Postoperative HO entwickelt sich am häufigsten nach Eingriffen, die eine offene Reposition, interne Fixierung und Gelenkersatzoperationen erfordern, wobei die HTEP am häufigsten vorkommt.
Reaktive Läsionen an Händen und Füßen sind in der Regel mit dem Periost oder periartikulärem fibrösem Gewebe assoziiert, was die Kategorie von der Myositis ossificans unterscheidet. Diese Läsionen treten in drei klinisch-radiologischen Settings auf: bizzare parosteale Osteochondrome

tous, floride reaktive Periitis und subunguale Exostosen.
Prävalenz
– Nach Amputation der unteren Extremitäten: 7%
– Nach einem Schädel-Hirn-Trauma: 11% (Schwankungsbreite von 10-20%)
Hüfte am häufigsten, gefolgt vom Ellenbogen
– Nach einem Schädel-Hirn-Trauma: 20% (Schwankungsbreite von 20-40%)
– Nach einer HTEP: 55%
– Nach einer Ellenbogenfraktur und/oder Dislokation: 90%
Nach einer Unterarmfraktur: 20%
In einer aktuellen Studie haben Foruria et al. untersuchten die Prävalenz der heterotopen Ossifikation bei allen Ellenbogenpathologien, die über einen Zeitraum von 5 Jahren in die Notaufnahme kamen. Sie fanden heraus, dass die höchste Prävalenz von HO bei schrecklichen Triad-Verletzungen, Transolekranonfraktur-Dislokationen und einer damit verbundenen distalen Humerusfraktur auftrat. Die Lage der Verknöcherung wurde am häufigsten auf dem hinteren Aspekt der Elle gefunden. Zu den Risikofaktoren für HO gehören eine Dislokation oder Subluxation zum Zeitpunkt der Verletzung, eine offene Verletzung und eine schwere Brustverletzung. Wenn eine Pathologie chirurgisch behandelt wurde, entwickelten 37 % der Teilnehmer eine Ossifikation.
Klinische Diagnose
Klinische Anzeichen und Symptome von HO können bereits 3 Wochen oder bis zu 12 Wochen nach dem ersten muskuloskelettalen Trauma, der Rückenmarksverletzung oder anderen auslösenden Ereignissen auftreten. Das erste Anzeichen von HO ist in der Regel der Verlust der Gelenkbeweglichkeit und anschließend der Funktionsverlust. Andere Befunde, die auf das Vorhandensein von HO hinweisen können, sind Schwellungen, Erythem, Hitze, lokale Schmerzen, tastbare Masse und Kontrakturbildung. In einigen Fällen kann auch Fieber vorhanden sein.
Differenzialdiagnosen: Die initiale Entzündungsphase der HO kann andere Pathologien wie Zellulitis, Thrombophlebitis, Osteomyelitis oder einen tumorösen Prozess imitieren. Andere Differentialdiagnosen umfassen TVT, septische Arthritis, Hämatom oder Fraktur. TVT und HO wurden positiv assoziiert. Es wird angenommen, dass dies auf den Masseneffekt und die lokale Entzündung der HO zurückzuführen ist, die die Thrombusbildung begünstigen. Die Thrombusbildung wird durch Venenkompression und Phlebitis verursacht.
Klassifikationssysteme
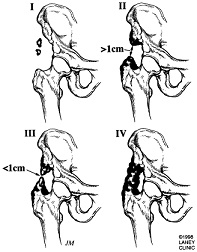
Brooker-Klassifikation der heterotopen Ossifikation (nach HTEP)
Klasse 1: Knocheninsel innerhalb eines Weichteilgewebes um die Hüfte
Klasse 2: Knochensporne, die vom Becken des proximalen Endes des Oberschenkelknochens ausgehen und mindestens 1 cm zwischen den gegenüberliegenden Knochenflächen lassen
Klasse 3: Knochensporne, die vom Becken oder dem proximalen Femur ausgehen und <1 cm zwischen den gegenüberliegenden Knochenoberflächen lassen
Klasse 4: Ankylosen der Hüfte
Brooker beschrieb keine Klasse 0, aber nachfolgende Studien, die die Brooker-Klassifikation verwenden, haben Klasse 0 als das Fehlen von röntgenologischem HO definiert.
Schmidt und Hackenbrock Klassifikation der heterotopen Ossifikation (nach HTEP)
Region 1: Heterotope Ossifikation streng unterhalb der Spitze des Trochanter major
Region 2: Heterotope Ossifikation unterhalb und oberhalb der Spitze des Trochanter major
Region 3: Heterotope Ossifikation streng oberhalb der Spitze des Trochanter major
Grad A: Einzelne oder multiple heterotope Ossifikation <10 mm in maximaler Ausdehnung ohne Kontakt mit Becken oder Femur
Grad B: Heterotopische Ossifikation >10 mm ohne Kontakt zum Becken, aber mit möglichem Kontakt zum Femur; keine Überbrückung vom Femur zum proximalen Teil des Trochanter major; kein Nachweis von Ankylosen
Grad C: Ankylose mit fester Überbrückung vom Femur zum Becken
McAfee’s Classification of Heterotopic Ossification (Following Total Disc Arthroplasty)
0: Keine HO
1: Knocheninseln nicht innerhalb der Ränder der Bandscheibe und keine Beeinträchtigung der Bewegung
2: Knochen innerhalb der Bandscheibenränder, der die Bewegung nicht behindert
3: Knochen innerhalb der Bandscheibenränder, der die Bewegung der Prothese behindert
4: Knochenankylose
Stadien der Entwicklung
Chronologie der Entwicklung der heterotopen Ossifikation
- 0 Tage: +/- Erythem, Schwellung, Zärtlichkeit
- 7 Tage: klinisch tastbare Masse
- 7-14 Tage: schlecht definierter Schatten auf dem Röntgenbild
- 14-21 Tage: Osteoidablagerungen, Röntgenschatten
- 21-35 Tage: flauschige Radiodensitäten; der „gepunktete Schleier“-Effekt
- 24 Tage: definitiver röntgenologischer Nachweis
- 30 Tage: Mineralisierung zeigt ein zonales Muster (am besten auf dem CT-Scan zu sehen)
- 45 Tage: histologisches „zonales“ Muster erkennbar, das eine gut ausgebildete Mineralisierung in der Peripherie widerspiegelt
- 180-365 Tage: Entwicklung von reifem Knochen
Diagnostische Tests und Labortests
Ultraschall

– Erkennung von HO 2 Wochen früher als durch Röntgen
– Genauer als jeder Labortest
– Hilft dem Arzt, sich für eine sofortige/aggressive physikalische Therapie einzusetzen
– Eliminiert die hohe Falsch-Positiv-Rate der physikalischen Untersuchung allein
– Dreiphasen-Knochenszintigraphie
– Diagnostische und therapeutische Nachsorgezwecke
– Die Phasen 1 und 2 zeigen Hyperämie und Blutansammlungen an (Vorläufer des HO-Prozesses)
– Normalerweise positiv nach 2-4 Wochen
– Serielle Knochenscans werden zur Überwachung der Stoffwechselaktivität der HO verwendet, um den optimalen Zeitpunkt für eine chirurgische Resektion zu bestimmen und das postoperative Auftreten vorherzusagen
Radiographie
– Weichteilmasse ist der früheste radiologische Befund
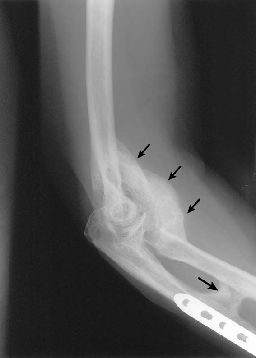
– HO, die auf Röntgenbildern 46 Wochen nach der Verletzung hat ein typisches Erscheinungsbild einer zirkumferentiellen Ossifikation mit einem durchscheinenden Zentrum
– Kann die Mineralisierung von HO in den ersten Wochen nach Trauma/Auftritt nicht erkennen
– Wird häufig zur Klassifizierung von HO nach HTEP verwendet
– Differentialdiagnosen: Abrissfrakturfragmente, osteochondrale Körper, nichtknöcherne Weichteilverkalkung und Osteosarkom
MRT und CT-Scan
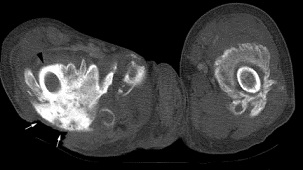
– MRT wird nicht routinemäßig zur Beurteilung von HO verwendet
– CT kann Weichteilverknöcherungen in früheren Stadien als Standard-Röntgenaufnahmen erkennen
Drei-Phasen-Technetium-99m (99mTc) Methylendiphosphonat-Knochenscan
– Empfindlichstes bildgebendes Verfahren zur Früherkennung und Beurteilung der Reife von HO
– Kann zur Überwachung der Stoffwechselaktivität von HO und zur Bestimmung des geeigneten Zeitpunkts für eine Operation sowie zur Vorhersage eines postoperativen Rezidivs verwendet werden
– Normalerweise positiv >2 Wochen vor dem radiologischen Nachweis von HO
Prostaglandin E2: (PGE2)
– Überwachen Sie die PGE2-Ausscheidung im 24-Stunden-Urin
– PGE2 gilt als zuverlässiger Knochenmarker für die Früherkennung und die Bestimmung der Behandlungseffektivität
– Ein plötzlicher Anstieg ist eine Indikation für eine Knochenszintigraphie
Alkalische Phosphatase: (ALP)
– Wird häufig zur Früherkennung von HO verwendet
ALP-Werte sind bei früher HO erhöht und erreichen nach ~4 Wochen ein Plateau
– Kann nicht verwendet werden, um klinische Rückschlüsse auf die Reife oder das Wiederauftreten von HO zu ziehen
– Akute Frakturen haben oft ähnliche ALP-Werte,
Erhöhte Kreatinkinase-Werte
– Korrelieren mit der histologischen Beteiligung des Muskels und dem Schweregrad der Erkrankung
– Nicht spezifisch für HO
– Kann ein höheres Risiko für die Entwicklung und den Schweregrad von HO vorhersagen
– Kann bei der Planung und Bewertung des Ansprechens auf die Behandlung hilfreich sein
Matrix Metalloproteinase-9
– Marine Tiermodelle legen nahe, dass dies ein früher Biomarker für die HO-Bildung sein könnte
Klinische Anmerkung: Der Mangel an einfachen objektiven Maßnahmen zur Erkennung von heterotoper Knochenbildung führt dazu, dass HO in den frühen Stadien fehldiagnostiziert wird, was zu einer verzögerten Behandlung führt.
Systemische Beteiligung
Es ist erwiesen, dass es keine systemischen Auswirkungen gibt, die mit der Bildung der heterotopen Ossifikation einhergehen. Die häufigsten Stellen, an denen dieser Zustand auftritt, sind die Hüfte, die Knie, die Wirbelsäule, der Ellenbogen, die Handgelenke, die Hände und jede Stelle, die in ein traumatisches Ereignis involviert ist.
Assoziierte Komorbiditäten
Die häufigsten Erkrankungen, die in Verbindung mit heterotoper Ossifikation auftreten, sind:
- Spondylitis ankylosans
- Rhuematoide Arthritis
- Hypertrophe Osteoarthritis
- Diffuse idiopathische skelettale Hyperostose
- Morbus Paget
- Quadriplegie und Paraplegie
Medizinisches Management (Current Best Evidence)
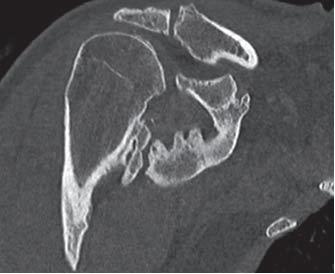
Die Behandlung der heterotopen Ossifikation ist weitgehend abhängig von der Menge der ektopen Knochenbildung, der Lokalisation und den damit verbundenen funktionellen Einschränkungen des Patienten.
Das erste Ziel des medizinischen Managements ist es, diejenigen Patienten zu identifizieren, die ein Risiko haben, eine HO zu entwickeln, und sie prophylaktisch zu behandeln. Die Forschung unterstützt zwei weitere Ansätze für das medizinische Management von HO: 1) chirurgische Exzision und 2) Strahlentherapie.
Prophylaktische Behandlung:
Auf diesem Gebiet muss noch weiter geforscht werden, allerdings gibt es derzeit experimentelle Optionen. Dazu gehören:
Lokale Strahlentherapie
- Verringerte Inzidenz aller Brooker-Klassen von HO nach THA, hat aber einen größeren Effekt auf die Verhinderung von Brooker-Klassifikation 3 und 4 im Vergleich zu NSAIDS
- Postoperativ besser als präoperativ
- Die Verwendung von Strahlentherapie als prophylaktische Behandlung stammt hauptsächlich aus der Literatur zur totalen Hüftarthroplastik.
- Die Bestrahlung von pluripotenten mesenchymalen Zellen kann die Entwicklung von HO effektiv verhindern.
- Eine Dosis von 700-800 cGy lokaler Bestrahlung in den ersten vier postoperativen Tagen hat gezeigt, dass sie die Bildung von HO bei Patienten mit hohem Risiko verhindert.
Orales Indomenthacin
Medikationen:
Medikamente werden Patienten, die ein Risiko für die Entwicklung einer heterotopen Ossifikation haben, zur Vorbeugung und zur Unterstützung der Behandlung nach der Bildung von heterotopen Läsionen verschrieben. Die beiden Arten von Medikamenten, die nachweislich sowohl einen prophylaktischen als auch einen therapeutischen Nutzen haben, sind folgende:
Nichtsteroidale Antirheumatika: NSAIDS
Indomethacin (zweifache Wirkung)
1. Hemmung der Differenzierung von mesenchymalen Zellen zu osteogenen Zellen (direkt)
2. Hemmung des posttraumatischen Knochenumbaus durch Unterdrückung der Prostaglandin-vermittelten Reaktion (indirekt) und entzündungshemmende Eigenschaften
Biphosphonate:
Dreifache Wirkung
1. Hemmung der Kalziumphosphatausfällung
2. Verlangsamung der Hydroxylapatit-Kristallaggregation
3. Hemmung der Umwandlung von Kalziumphosphat zu Hydroxylapatit
Klinischer Hinweis: Kliniker müssen sich bei Patienten, die routinemäßig NSAIDS einnehmen, der möglichen Komplikationen (hauptsächlich im Zusammenhang mit dem Magen-Darm-Trakt) bewusst sein.
Sugische Intervention:
Die beiden Hauptziele der chirurgischen Intervention sind die Veränderung der Position des betroffenen Gelenks oder die Verbesserung seines Bewegungsumfangs (ROM). Durch seine Arbeit hat Garland einen empfohlenen Zeitplan für chirurgische Eingriffe erstellt:
- 6 Monate nach der traumatischen Entwicklung von HO
- 1 Jahr nach der Entwicklung von HO sekundär zu einer Rückenmarksverletzung
- 18 Monate nach der Entwicklung von HO sekundär zu einer Kopfverletzung
Die oben genannten Zeitpläne wurden erstellt, um den optimalen Zeitpunkt für einen chirurgischen Eingriff zu bestimmen. Kliniker müssen vor der chirurgischen Exzision feststellen, ob die Läsion die Reifung erreicht hat, um das Risiko von intraoperativen Komplikationen wie Blutungen und das Wiederauftreten der ektopischen Läsion zu verringern. Die Verwendung von Knochenscans zur Bestimmung der Stoffwechselaktivität der Läsion und der Serum-ALP-Spiegel sind gängige Hilfsmittel in diesem Entscheidungsprozess.

Shehab et al. beschreibt Kriterien für die Empfehlung der chirurgischen Entfernung einer heterotopen Ossifikation. Die Kriterien sind wie folgt:
- Signifikant eingeschränktes ROM des betroffenen Gelenks (z.B. sollte die Hüfte < 50 Grad ROM haben) für die meisten Patienten, das Fortschreiten zur Gelenkankylose ist die schwerwiegendste Komplikation der heterotopen Ossifikation.
- Abwesenheit von lokalem Fieber, Schwellung, Erythem oder anderen klinischen Befunden einer akuten heterotopen Ossifikation.
- Normale alkalische Phosphatwerte im Serum.
- Rückkehr der Knochenscan-Befunde in den Normalbereich oder in die Nähe des Normalbereichs; wenn serielle quantitative Knochenscans durchgeführt werden, sollte es einen stark abnehmenden Trend geben, gefolgt von einem stabilen Zustand für 2-3 Monate.
Rehabilitation nach der Operation
Es wird empfohlen, dass ein Rehabilitationsprogramm innerhalb der ersten 24 Stunden nach der Operation begonnen wird. Das Programm sollte 3 Wochen dauern, um Adhäsionen vorzubeugen.
Physikalisches Therapiemanagement
Physikalische Therapie hat sich bei Patienten mit heterotoper Ossifikation als vorteilhaft erwiesen. Präoperative PT kann helfen, die Strukturen um die Läsion herum zu präparieren. ROM-Übungen (PROM, AAROM, AROM) und Kräftigung helfen, Muskelatrophie zu verhindern und die Gelenkbewegung zu erhalten.
Klinischer Hinweis: Bei Patienten mit bekannten heterotopen Läsionen ist Vorsicht geboten. Eine zu aggressive Therapie kann den Zustand verschlimmern und zu Entzündungen, Erythemen, Blutungen und verstärkten Schmerzen führen.
Eine postoperative Rehabilitation hat sich auch bei Patienten mit kürzlich erfolgter chirurgischer Resektion einer heterotopen Ossifikation als vorteilhaft erwiesen. Das postoperative Management von HO ist ähnlich wie die präoperative Behandlung, aber es wird viel mehr Wert auf Ödemkontrolle, Narbenmanagement und Infektionsprävention gelegt. Calandruccio et al. skizzierten ein Rehabilitationsprotokoll für Patienten, die sich einer chirurgischen Exzision einer heterotopen Ossifikation des Ellenbogens unterzogen haben. Die Phasen der Reha und die Ziele für jede Phase sind wie folgt:
Phase I (Woche 1)
Ziele:
- Infektionen vorbeugen
- Schutz und Verringerung der Belastung der Operationsstelle
- Schmerzreduktion
- Kontrolle und Verringerung des Ödems
- ROM bis 80% des betroffenen Gelenks
- Erhalt des ROM des Gelenks proximal und distal der Operationsstelle
Phase II (2-8 Wochen)
Ziele:
- Schmerz reduzieren
- Ödeme kontrollieren
- Eingeschränkte ADL-Leistungen fördern
- Mobilität der Narbe und richtige Remodellierung fördern
- Vollständige ROM des betroffenen Gelenks
- Fördern Sie hochwertige Muskelkontraktionen
 Foto mit freundlicher Genehmigung von prosportscare.com
Foto mit freundlicher Genehmigung von prosportscare.com
Phase III (9-24 Wochen)
Ziele:
- Selbstmanagement der Schmerzen
- Vorbeugung von Flare-
- Kraft verbessern
- ROM verbessern (falls noch eingeschränkt)
- Rückkehr zum vorherigen Aktivitätsniveau
Casavant und Hastings geben in ihrem Artikel „Heterotopic Ossification about the Elbow“ (Heterotopische Ossifikation am Ellenbogen) ebenfalls einen guten Einblick in die Bewertung und Behandlung von heterotopen Ossifikationen: A Therapist’s Guide to Evaluation and Management.
Klinische Anmerkung: Die beiden oben verwendeten Studien konzentrierten sich in erster Linie auf die Rehabilitation des Ellenbogens als Folge einer heterotopen Ossifikation. Die Ziele und Phasen des Rehabilitationsprozesses können jedoch als Leitfaden für die Behandlung an anderen Stellen verwendet werden.
Fallbericht
Titel: Heterotope Ossifikation mit Radikulopathie nach lumbaler Bandscheiben-Totalendoprothese
Schlüsselwörter: Heterotope Ossifikation, physikalische Therapie, totale Bandscheibenarthroplastik, Radikulopathie
Word Count: 520
Autoren: Keith L. Jackson, Justin M. Hire, Jeremy M. Jacobs, Charles C. Key und John G. DeVine (modifiziert von Morgan Blake und Hannah McCabe)
Abstract:
Dieser Fall beschreibt die Komplikationen, die ein Mann aufgrund der Entwicklung einer postoperativen heterotopen Ossifikation in seiner Lendenwirbelsäule erlebte.
Einleitung:
Die Bandscheibentotalendoprothese ist eine relativ neue Behandlungsstrategie bei lumbalen diskogenen Rückenschmerzen, die kurz- und mittelfristig vielversprechende Ergebnisse gezeigt hat. Zu den spezifischen Komplikationen, die mit einer Bandscheibentotalendoprothese einhergehen können, gehören Wirbelkörperfrakturen, heterotope Ossifikation (HO), Implantatfehlstellung und frühe oder späte Komponentenextrusion. Dieser Fall beschreibt eine posteriore Komponentenplatzierung, die zu heterotopem Knochenwachstum innerhalb des Wirbelkanals führte, was ein neurales Impingement und eine Radikulopathie verursachte und schließlich eine Komponentenextraktion, Dekompression und lumbale Arthrodese erforderte.
Falldarstellung:
- Subjektiv: Ein 45-jähriger Mann stellt sich in der Klinik mit neu aufgetretenen Schmerzen im rechten Bein vor. Er verneint Parästhesien oder den Verlust der motorischen Funktion, und er verneint auch eine Vorgeschichte von HO-Bildung, Trauma oder entzündlicher Arthritis. Seine PMH umfasst eine lumbale Bandscheiben-Totalendoprothese an L5/S1 vor 2 Jahren wegen diskogener Rückenschmerzen. Er berichtet, dass er nach der Operation eine deutliche Verringerung seiner Symptome hatte, aber vor etwa 6 Monaten diese neuen Schmerzen entwickelte.
- Demographische Informationen: 45 Jahre alt, männlich, arbeitet für UPS als Postzusteller
- Medizinische Diagnose: Verdacht auf HO
- Komorbiditäten: HTN, DM
- Vorherige Versorgung/Behandlung: Physiotherapie (minimale Verbesserungen wurden festgestellt)
- Selbstberichtsergebnisse: Oswestry: 46% (Schwere Behinderung)
- Objektiv: Die körperliche Untersuchung ergab ein eingeschränktes lumbales ROM in Vorwärtsbeugung aufgrund von Schmerzen im rechten Bein, einen positiven Einbein-Hebetest, eine Kraft von 5/5 für alle Hauptmuskelgruppen, ein intaktes Gefühl und normale (2+) Reflexe.
Der Patient wurde an seinen Hausarzt überwiesen, der zusätzliche Tests durchführte. Die Ergebnisse der zusätzlichen Tests waren:
- Röntgenaufnahmen zeigten ein Eindringen des Implantats in den Wirbelkanal mit heterotoper Knochenbildung außerhalb der Ränder der Bandscheibe.
- Das Computertomographie-Myelogramm zeigte eine Kompression der traversierenden Nervenwurzel als Folge der inferioren Endplatte des Implantats, die sich hinter dem Rand der Wirbelendplatte befand, sowie ein damit verbundenes posteriores Knochenwachstum weiter in den Kanal hinein.
Klinischer Eindruck:
Der Patient weist ein vermindertes lumbales ROM auf, mit einer Vorgeschichte eines Traumas der Lendenwirbelsäule aufgrund der lumbalen Bandscheibenprothese. Diese Faktoren und die positive Bildgebung führten dazu, dass der Patient mit HO diagnostiziert wurde.
Intervention:
Der Patient entschied sich für die operative Entfernung seiner lumbalen Arthroplastik mit Fusion von L5/S1 und HO-Dekompression. Der Patient kehrte postoperativ zur Physiotherapie zurück, um sich zu erholen.
Ergebnisse:
6 Wochen postoperativ berichtet der Patient über eine vollständige Linderung seiner radikulären Beinschmerzen. Die Röntgenbilder zeigen eine solide Fusion ohne Rezidiv der HO-Bildung.
Diskussion:
Als Physiotherapeut ist es wichtig, HO in der Differentialdiagnose zu berücksichtigen, wenn man Patienten mit einer Vorgeschichte von Trauma oder Operation behandelt. Es ist besonders wichtig, die Anzeichen und Symptome von HO zu beachten, wenn man Patienten mit eingeschränktem ROM behandelt. Wir sind vielleicht die ersten Mediziner, die die Entwicklung von HO erkennen.
Dankeschön:
Fall adaptiert aus „Heterotopic Ossification Causing Radiculopathy after Lumbar Total Disc Arthroplasty“
Case Studies
Tibiofibuläre Syndesmose und Ossifikation. Fallbericht: Folgen einer Knöchelverstauchung bei einem jugendlichen Fußballspieler.
- Kennedy MA, Sama AE, Sigman M. Tibiofibular syndesmosis and ossification. case report: sequelae of ankle sprain in an adolescent football player. Journ of Emer Med 2000; 18: 233-240.
Heterotopische mesenteriale Ossifikation („intraabdominale Myositis ossificans): A Case Report.
- Bovo G, Romano F, Perego E, Franciosi C et al. Heterotopic mesenteric ossification („intraabdominal myositis ossificans“): a case report. International Journal of Surgical Pathology 2004; 12: 407-409.
Ein Fall von Psoas-Ossifikation nach Verwendung von BMP-2 für die posterolaterale Fusion bei L4-L5.
- Brower RS, Vickroy NM. A case of psoas ossification from the use of BMP-2
for posterolateral fusion at L4-L5.Spine 2008; 18: 653-655.<span />
Infrapatellare heterotope Ossifikation nach Rekonstruktion des vorderen Kreuzbandes.
- Valencia H, Gavín C. Infrapatellare heterotope Ossifikation nach anteriorer Kreuzbandrekonstruktion. Knee Surgery, Sports Traumatology, Arthroscopy: Official Journal Of The ESSKA ; 15(1): 39-42. Available from: MEDLINE.]
Heterotope Ossifikation des ulnaren Seitenbandes: Die Beschreibung eines Falles bei einem Spitzenathleten im Gewichtheben.
- A Giombini, L Innocenzi, G Massazza, F Fagnani, et al. Heterotopic ossification of the ulnar collateral ligament: a description of a case in a top level weightlifting athlete. Zeitschrift für Sportmedizin und körperliche Fitness. 2005 Sep 1;45(3): 370-80. In: ProQuest Medical Library . Verfügbar unter: ProQuest; Document ID: 942792311]
Ressourcen
Das Geheimnis der heterotopen Ossifikation und wie sie mein Leben beeinflusste
- 1.00 1.01 1.02 1.03 1.04 1.05 1.06 1.07 1.08 1.09 1.10 1.11 1.12 1.13 1.14 Mavrogenis AF, Soucacos PN, Papagelopoulos PJ. Heterotopische Ossifikation Revisited. Orthopedics. 2011Jan;34(3):177.
- 2.0 2.1 2.2 2.3 2.4 2.5 McCarthy EF, Sundaram M. Heterotopic ossification: a review. Skeletal Radiol 2005; 34: 609-619.
- 3.0 3.1 3.2 3.3 3.4 3.5 3.6 Firoozabadi R, Alton T, Sagi HC. Heterotopische Ossifikation in der Acetabulumfrakturchirurgie. Journal of the American Academy of Orthopaedic Surgeons. 2017;25(2):117-24.
- 4.0 4.1 4.2 4.3 4.4 4.5 Bossche LV, Vanderstraeten G. Heterotopic ossification: a review. J Rehabil Med 2005; 37: 129-136.5. Pape HC et al. Aktuelle Konzepte bei der Entstehung der hetetrotopen Ossifikation. Journ Bone and Joint Surg 2004; 86: 783-787.
- 5.0 5.1 5.2 5.3 Pape HC et al. Current concepts in the development of hetetrotopic ossification. Journ Bone and Joint Surg 2004; 86: 783-787.
- 6.0 6.1 6.2 6.3 6.4 6.5 6.6 6.7 Hsu JE, Keenan MA. Current review of heterotopic ossification. UPOJ 2010; 20: 126-130.
- 7.0 7.1 7.2 7.3 7.4 Foruria AM, Augustin S, Morrey BF, Sanchez-Sotelo Joaquin. Heterotope Ossifikation nach chirurgischen Eingriffen bei Frakturen und Fraktur-Dislokationen, die die proximale Seite des Radius oder der Ulna betreffen. The Journal of Bone and Joint Surgery, Incorporated. 2015May15;95-A(10):e66(1)-e66(7).
- 8.0 8.1 Dalury DF, Jiranek WA. Die Inzidenz der heterotopen Ossifikation nach einer Knietotalendoprothese. Journal of Arthroplasty 2004; 19: 447-457.
- 9.0 9.1 9.2 Shehab D, Elgazzar AH, Collier BD. Heterotopic ossification. Jour of Nuclear Medicine 2002; 43: 346-353.
- Hug KT, Alton TB, Gee AO. In Brief: Classifications in Brief: Brooker Classification of Heterotopic Ossification After Total Hip Arthroplasty. Clinical Orthopaedics and Related Research®. 2014;473(6):2154-7.