INTRODUIRE LES ANHYDRIDES D’ACIDE
Cette page explique ce que sont les anhydrides d’acide et examine leurs propriétés physiques simples telles que les points d’ébullition. Elle présente leur réactivité chimique de manière générale, mais les détails des réactions spécifiques sont donnés sur des pages séparées – voir le menu des anhydrides d’acide (lien en bas de page).
Que sont les anhydrides d’acide ?
La structure des anhydrides d’acide
Un acide carboxylique comme l’acide éthanoïque a la structure suivante :
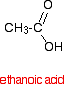
Si vous preniez deux molécules d’acide éthanoïque et que vous enleviez une molécule d’eau entre elles, vous obtiendriez l’anhydride d’acide, l’anhydride éthanoïque (ancien nom : anhydride acétique).
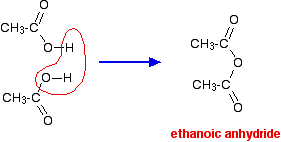
On peut effectivement fabriquer de l’anhydride éthanoïque en déshydratant de l’acide éthanoïque, mais on le fabrique normalement d’une manière plus efficace et détournée. (La fabrication de l’anhydride éthanoïque dépasse le cadre du niveau A britannique.)
Nommer les anhydrides d’acide
C’est très facile. Il suffit de prendre le nom de l’acide parent, et de remplacer le mot « acide » par « anhydride ». » Anhydride » signifie simplement » sans eau « .
Donc… l’acide éthanoïque forme l’anhydride éthanoïque ; l’acide propanoïque forme l’anhydride propanoïque, et ainsi de suite.
Pour les besoins du niveau A britannique, le seul que vous êtes du tout susceptible de rencontrer est l’anhydride éthanoïque.
Propriétés physiques des anhydrides d’acide
Nous prendrons l’anhydride éthanoïque comme typique.
Apparence
L’anhydride éthanoïque est un liquide incolore, sentant fortement le vinaigre (acide éthanoïque).
L’odeur est due au fait que l’anhydride éthanoïque réagit avec la vapeur d’eau présente dans l’air (et l’humidité de votre nez) pour produire à nouveau de l’acide éthanoïque. Cette réaction avec l’eau est donnée en détail sur une autre page. (Trouvez-la dans le menu des anhydrides d’acide – lien en bas de cette page.)
Solubilité dans l’eau
On ne peut pas dire que l’anhydride éthanoïque se dissout dans l’eau car il réagit avec elle pour donner de l’acide éthanoïque. Il n’existe pas de solution aqueuse d’anhydride éthanoïque.
Point d’ébullition
L’anhydride éthanoïque bout à 140°C. Cela s’explique par le fait que c’est une assez grosse molécule polaire et qu’elle possède donc à la fois des forces de dispersion de van der Waals et des attractions dipôle-dipôle.
Elle ne forme cependant pas de liaisons hydrogène. Cela signifie que son point d’ébullition n’est pas aussi élevé que celui d’un acide carboxylique de taille similaire. Par exemple, l’acide pentanoïque (l’acide de taille la plus similaire) bout à 186°C.
.