A.M.C. Davies
Norwich Near Infrared Consultancy, 10 Aspen Way, Cringleford, Norwich NR4 6UA, UK
Als je je hand naar een brandend vuurtje uitsteekt, “voel” je de warmte die het vuur afgeeft, maar wat gebeurt er eigenlijk? Het vuur geeft licht en infrarode (IR) straling af; van een vuur is het grootste deel bijna-infrarode (NIR) straling. Een deel van de NIR-straling wordt geabsorbeerd door watermoleculen in uw huid. Dit verhoogt de temperatuur van het water en resulteert in een temperatuurstijging in het omringende weefsel, die wordt waargenomen door zenuwen in uw huid. Deze straling werd in 1800 ontdekt door William Herschel, een musicus en zeer succesvol amateur-astronoom (hij ontdekte de planeet Uranus), omdat hij wilde weten of een bepaalde kleur geassocieerd werd met warmte van zonlicht. Hij ontdekte dat het warmtemaximum voorbij het rode eind van het spectrum lag. Herschel kon niet geloven dat licht en zijn “stralingswarmte” met elkaar in verband stonden, maar hij had het mis. In 1835 had Ampere aangetoond dat het enige verschil tussen licht en wat hij “infrarode straling” noemde, hun golflengte was. In 1864 schreef James Maxwell: “Deze snelheid komt zo dicht in de buurt van die van licht, dat het lijkt alsof we sterke redenen hebben om te concluderen dat het licht zelf (met inbegrip van stralingswarmte en andere stralingen) een elektromagnetische storing is in de vorm van golven die zich voortplanten door het elektromagnetische veld volgens de elektromagnetische wetten”. Wat wij nu het elektromagnetisch spectrum noemen, is weergegeven in figuur 1.

Eerdere geschiedenis van de studie van infraroodabsorpties
De eerste (nabij) infraroodspectra werden in 1881 gemeten door Abney en Festing met behulp van fotografische platen. Niet alleen produceerden zij de eerste spectra, maar zij suggereerden ook, terecht, dat de absorpties verband hielden met de chemische samenstelling van de vloeistoffen die zij onderzochten. De belangrijkste pionier van de IR-spectroscopie was William W. Coblentz. In 1905 publiceerde hij het resultaat van een grote studie van verbindingen waarvan hij de spectra had opgenomen van 1000 nm tot 16.000 nm. Coblentz’ werk betekende een doorbraak in die zin dat onderzoekers in staat waren het karakter van groepen atomen binnen moleculen in verband te brengen met specifieke absorpties in het midden-IR (2500-50.000 nm). Deze absorpties zijn het resultaat van interacties met de fundamentele trillingen van de chemische bindingen die verbonden zijn met de atomen van de groepen. We kunnen chemische bindingen beschouwen als zwakke veren die twee of meer atomen bijeenhouden, deze veren zullen op natuurlijke wijze trillen en wanneer er energie aan het systeem wordt toegevoegd, zullen ze energetischer gaan trillen. Atomen in moleculen worden echter beperkt door de kwantummechanica, zodat slechts een paar specifieke energieniveaus zijn toegestaan. Als er slechts twee atomen zijn, zal de enige trilling worden gezien als een uitrekking. Als er drie of meer atomen bij betrokken zijn, kunnen bindingen ook buigen, waardoor een hele reeks verschillende trillingen ontstaat. Voor strekvibraties is meer energie nodig dan voor buigtrillingen, maar er zal ook variatie zijn in de energiebehoefte van de buigtrillingen. Verschillende chemische bindingen (zoals O-H, C-H en N-H) verschillen in sterkte en dus in de hoeveelheid energie die nodig is om de bindtrilling van het ene niveau naar het volgende te brengen. Deze variatie in energie wordt in een spectrum zichtbaar als een reeks absorpties bij verschillende golflengtes. Door naar het spectrum te kijken kan men afleiden welke trillingen er optreden en zo de structuur van het molecuul (of de aanwezige groepen atomen) bepalen.
Een van de zeer nuttige eigenschappen van midden-IR-spectra is dat het gebied van 8500 nm tot 12.500 nm zeer karakteristiek is voor het gemeten molecuul en dit gebied staat bekend als het “vingerafdruk”-gebied omdat het kan worden gebruikt om de identiteit van veel zuivere stoffen te bevestigen. Terwijl de studie van mid-IR spectroscopie bleef groeien, vooral na de Tweede Wereldoorlog, bleef de belangstelling voor het NIR beperkt tot kwantitatieve metingen van water, enkele eenvoudige organische verbindingen en een zeer gering aantal studies van specifieke eiwitten. Niemand vond het nuttig voor het karakteriseren van monsters en het werd te complex geacht voor gebruik in kwantitatieve analyses.
Absorpties in het NIR-gebied
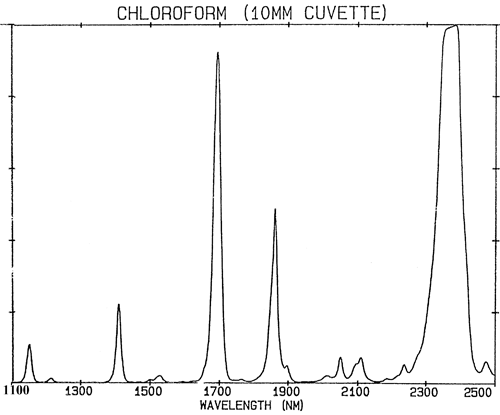
Als chemische bindingen zich precies als zwakke veren zouden gedragen, zou de kwantummechanica hun trilling tot slechts twee toestanden beperken en zouden er zeer weinig absorpties in het NIR-gebied zijn. Absorpties in het NIR-gebied (780-2500 nm) worden gegenereerd uit fundamentele trillingen door twee processen: boventonen en combinaties. Boventonen kunnen worden gezien als harmonischen. Zo zal elke grondtoon een reeks absorpties produceren op (ongeveer gehele) veelvouden van de frequentie (de frequentie is de reciproke van de golflengte). Combinaties zijn complexer. NIR-absorpties zijn in een hogere staat van opwinding, zodat zij meer energie vergen dan een fundamentele absorptie. Combinaties ontstaan door het delen van NIR-energie tussen twee of meer fundamentele absorpties. Hoewel het aantal mogelijke boventonen van een groep fundamentele absorpties in een molecuul beperkt is tot een paar, zal een zeer groot aantal combinaties worden waargenomen. Het effect van al deze absorpties samen maakt dat veel NIR-spectra er nogal oninteressant uitzien en slechts uit een paar tamelijk brede pieken bestaan. Figuur 2 is een NIR-spectrum van chloroform, CHCl3, het molecuul bevat slechts één waterstofatoom maar alle absorptie in zijn spectrum wordt veroorzaakt door dit ene atoom.
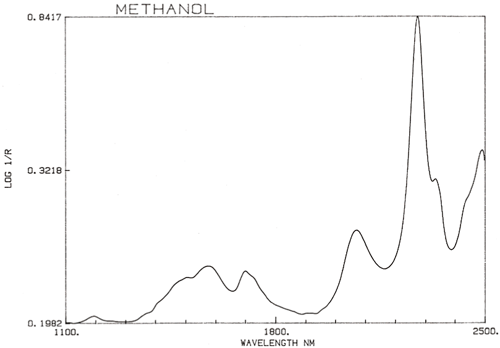
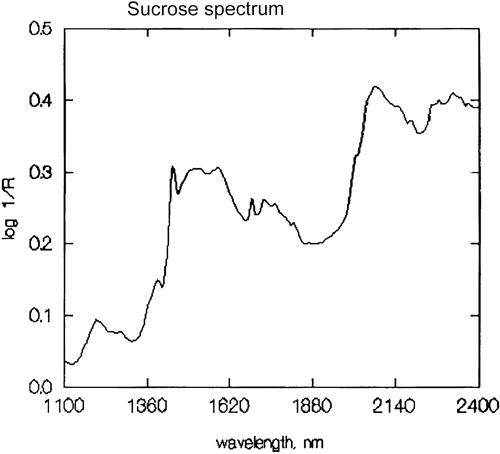
Het is een belangrijke generalisatie dat NIR-spectroscopie wordt gedomineerd door waterstof. Figuur 3 is een spectrum van methanol, CH3OH, dat vier waterstofatomen bevat (maar waarvan er drie equivalent zijn) en dit spectrum lijkt veel meer op een typisch NIR-spectrum met brede pieken. Figuur 4 is een spectrum van sucrose, C12H24O12, dat zeer brede absorptiegebieden vertoont, maar ook enkele vrij smalle pieken. Het is belangrijk te beseffen dat al deze brede absorpties worden veroorzaakt door meerdere smalle, elkaar overlappende absorpties. NIR-spectra zijn veel complexer dan ze lijken.
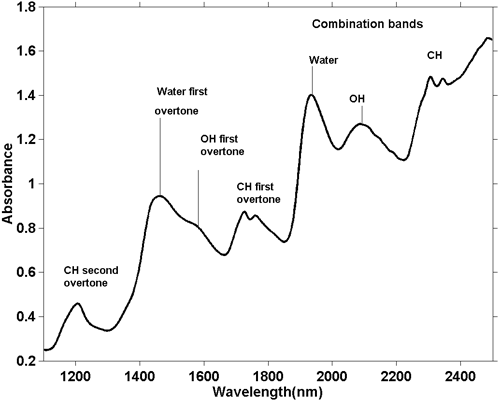
Hoewel NIR-spectra gecompliceerder zijn, is het toch mogelijk om enkele algemene waarnemingen te doen. Aangezien een fundamentele O-H-rekkende absorptie anders is dan een fundamentele C-H-rekkende, zal de reeks boventonen die door deze absorpties wordt gegenereerd, ook anders zijn. Hetzelfde geldt voor combinatiebanden. De meest voorkomende (en energetische) combinatiebanden ontstaan door strek- en buigcombinaties in dezelfde groep. Zo zien we absorpties door de combinatie van O-H rek met O-H buiging en C-H rek met C-H buiging en deze komen op verschillende posities in het spectrum voor. Figuur 5 is het NIR-spectrum van een koekjesdeegmonster. Biscuitdeeg bevat verschillende ingrediënten die elk veel verschillende moleculen bevatten, zodat dit spectrum honderden, zo niet duizenden absorpties bevat, maar we zien de integratie van ze allemaal en er lijken slechts een paar brede absorpties te zijn. Aan de hand van hun positie kunnen we in grote lijnen zeggen wat de oorzaak van de absorptie is, zoals aangegeven op de figuur.
Toen men zich voor het eerst bewust werd van de complexiteit van NIR-absorptie en dit vergeleek met de relatief gemakkelijker te begrijpen midden-IR-spectra, dachten de meeste onderzoekers dat er weinig te winnen viel met de bestudering van NIR-spectroscopie. Het gebied werd verwaarloosd en studenten kregen ten onrechte de instructie dat er niets te winnen viel bij het bestuderen van het NIR-gebied. Veel studenten wordt nog steeds dezelfde opvatting bijgebracht. De vereisten waren: spectrometers met zeer weinig ruis, de elektronische computer, de toepassing van wiskundige technieken (chemometrie) en een genie om dit alles samen te brengen. Die man was Karl Norris; een ingenieur die voor de USDA in Beltsville werkte. Hij had geen les gehad in spectroscopie en wist dus niet dat er in het NIR-gebied niets te winnen viel. Dus net als Herschel, die iets zocht waar niets was, ontwikkelde Norris de instrumenten en gebruikte hij computers om aan te tonen dat het NIR-gebied zeer nuttig was voor kwantitatieve analyse, met name van landbouwmonsters. Een van de redenen waarom NIR-analyse zo nuttig is, is dat het gebruik kan maken van gereflecteerde energie en dit betekent dat NIR-analyse kan worden gedaan met weinig of geen monstervoorbereiding. Gereflecteerde energie is complex. Ten eerste omdat er twee componenten zijn, speculaire (of spiegelachtige) en diffuse. In de context van NIR-spectroscopie geeft de speculaire component geen informatie. De diffuse component is afhankelijk van de fysische aard van het monster; vooral de deeltjesgrootte is van belang. Variatie van de fysische parameters van een monster veroorzaakt veranderingen in het spectrum, zodat het waargenomen spectrum een mengsel is van chemische en fysische informatie.
Het gebruik van gereflecteerde energie werd Karl Norris opgedrongen. Hoewel het de NIR-analyse van een veel breder scala van monsters mogelijk maakt, voegt het wel een extra laag complicaties toe. Een volledige wiskundige theorie van de reflectiespectroscopie is nog niet beschikbaar, maar door goede experimentele praktijken en het gebruik van wiskundige technieken is het mogelijk gebleken NIR-reflectiespectroscopie voor analytische chemie te gebruiken. Omdat de techniek kan worden toegepast met weinig of geen monstervoorbereiding, worden de analysetijden teruggebracht van uren tot minuten en bovendien kunnen uit dezelfde NIR-gegevens verschillende analyseresultaten worden verkregen, terwijl voor de conventionele analyse vaak een andere techniek en meer uren werk nodig zouden zijn. Het is echter noodzakelijk kalibraties te ontwikkelen die vele monsters, vele uren werk en duizenden (of waarschijnlijk miljoenen) computerberekeningen vergen. Met dit soort eigenschappen is het niet verwonderlijk dat 40 jaar na het baanbrekende onderzoek een zeer breed scala van analyses met NIR-spectroscopie kan worden verricht.
Wat wel verwonderlijk is, is dat ondanks het succes van NIR-spectroscopische analyse er wereldwijd maar zeer weinig universitaire scheikunde-afdelingen zijn die enig onderzoeksprogramma op het gebied van NIR-spectroscopie hebben. Bijgevolg verlaat het merendeel van de scheikundestudenten de universiteit zonder enige kennis van NIR, mogelijk met uitzondering van de ouderwetse opvatting dat er niets nuttigs te leren valt over het NIR-gebied.