Obiettivi di apprendimento
- Nominare gli acidi carbossilici con nomi comuni.
- Nominare gli acidi carbossilici secondo la nomenclatura IUPAC.
Gli acidi carbossilici si trovano ampiamente in natura, spesso combinati con alcoli o altri gruppi funzionali, come nei grassi, oli e cere. Sono componenti di molti alimenti, medicine e prodotti per la casa (Figura \(\PageIndex{1})). Non sorprende che molti di loro siano meglio conosciuti con nomi comuni basati su parole latine e greche che descrivono la loro fonte.
L’acido carbossilico più semplice, l’acido formico (HCOOH), fu ottenuto per la prima volta dalla distillazione delle formiche (latino formica, che significa “formica”). I morsi di alcune formiche iniettano acido formico, e le punture delle vespe e delle api contengono acido formico (così come altri materiali velenosi).

Il prossimo omologo superiore è l’acido acetico, che si ottiene dalla fermentazione di sidro e miele in presenza di ossigeno. Questa fermentazione produce l’aceto, una soluzione contenente il 4%-10% di acido acetico, più una serie di altri composti che aggiungono al suo sapore. L’acido acetico è probabilmente l’acido debole più familiare usato nei laboratori didattici e di chimica industriale.
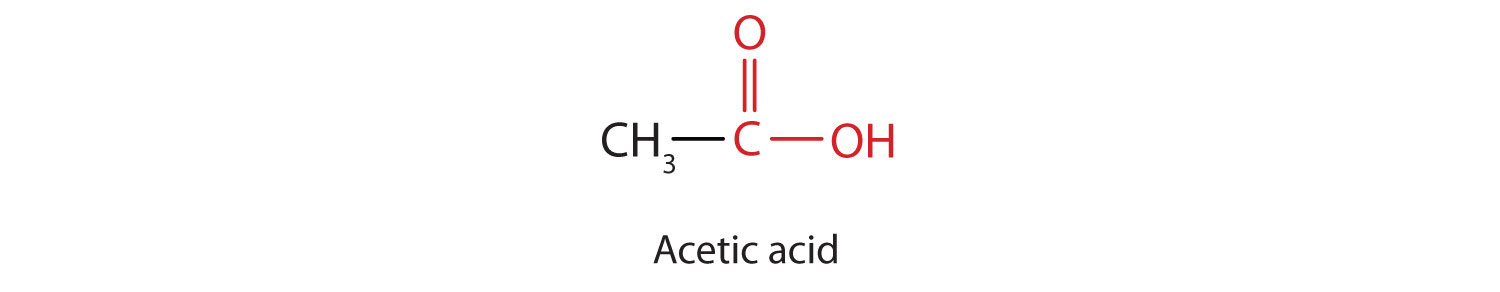
L’acido acetico puro solidifica a 16,6°C, solo leggermente al di sotto della normale temperatura ambiente. Nei laboratori scarsamente riscaldati della fine del XIX e dell’inizio del XX secolo nel Nord America e in Europa, l’acido acetico spesso “gelava” sul ripiano di stoccaggio. Per questa ragione, l’acido acetico puro (a volte chiamato acido acetico concentrato) era conosciuto come acido acetico glaciale, un nome che sopravvive ancora oggi.
Il terzo omologo, l’acido propionico (CH3CH2COOH), si incontra raramente nella vita quotidiana. Il quarto omologo, l’acido butirrico (CH3CH2CH2COOH), è una delle sostanze più maleodoranti che si possano immaginare. Si trova nel burro rancido ed è uno degli ingredienti dell’odore del corpo. Riconoscendo quantità estremamente piccole di questa e altre sostanze chimiche, i segugi sono in grado di rintracciare i fuggitivi. I modelli dei primi quattro acidi carbossilici sono mostrati nella figura \(\PageIndex{2}\).
L’acido con il gruppo carbossilico attaccato direttamente ad un anello benzenico è chiamato acido benzoico (C6H5COOH).

I nomi comuni degli acidi carbossilici usano lettere greche (α, β, γ, δ, e così via), non numeri, per designare la posizione dei gruppi sostituenti negli acidi. Queste lettere si riferiscono alla posizione dell’atomo di carbonio in relazione all’atomo di carbonio carbossilico.
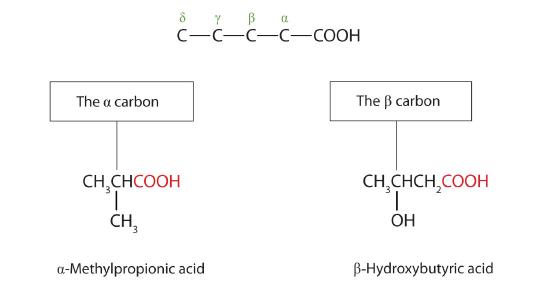
Nel sistema di nomenclatura dell’Unione internazionale di chimica pura e applicata (IUPAC), l’idrocarburo padre è quello che corrisponde alla catena continua più lunga (LCC) contenente il gruppo carbossilico. La desinenza -e dell’alcano padre è sostituita dal suffisso -oic e dalla parola acid. Per esempio, l’acido carbossilico derivato dal pentano è l’acido pentanoico (CH3CH2CH2CH2COOH). Come per le aldeidi, l’atomo di carbonio carbossilico è contato per primo; i numeri sono usati per indicare qualsiasi atomo di carbonio sostituito nella catena madre.
Le lettere greche sono usate con i nomi comuni; i numeri sono usati con i nomi IUPAC.
Esempio \(\PageIndex{1})
Dare i nomi comuni e IUPAC per ogni composto.
- ClCH2CH2CH2COOH
-
Soluzione
- L’LCC contiene quattro atomi di carbonio; il composto è quindi chiamato acido butirrico (o butanoico) sostituito.
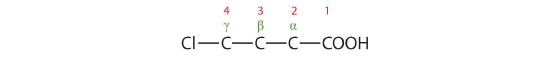
L’atomo di cloro è attaccato al carbonio γ nel sistema comune o C4 nel sistema IUPAC. Il composto è l’acido γ-clorobutirrico o acido 4-clorobutanoico.
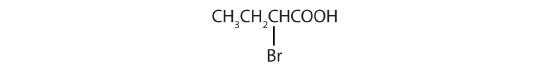
- L’LCC contiene quattro atomi di carbonio; il composto è quindi chiamato acido butirrico (o butanoico) sostituito.
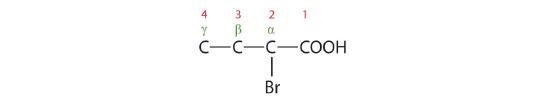
L’atomo di bromo (Br) è al carbonio α nel sistema comune o C2 nel sistema IUPAC. Il composto è l’acido α-bromobutirrico o l’acido 2-bromobutanoico.
Esercizio \(\PageIndex{1})
Dare il nome IUPAC per ogni composto.
- ClCH2CH2CH2CH2COOH
- (CH3)2CHCH2CHBrCOOH
Esempio \(\PageIndex{2})
Scrivi la formula strutturale condensata dell’acido β-cloropropionico.
Soluzione
L’acido propionico ha tre atomi di carbonio: C-C-COOH. Attacca un atomo di cloro (Cl) alla catena madre all’atomo di carbonio beta, il secondo dal gruppo carbossilico: Cl-C-C-COOH. Poi aggiungi abbastanza atomi di idrogeno per dare ad ogni atomo di carbonio quattro legami: ClCH2CH2COOH.
Esercizio \(\PageIndex{2})
Scrivi la formula strutturale condensata dell’acido 4-bromo-5-metilesanoico.
Esercizi di ripasso dei concetti
- Qual è il nome IUPAC dell’acido carbossilico a catena lineare con sei atomi di carbonio?
- L’aldeide a catena lineare con cinque atomi di carbonio ha il nome comune valeraldeide. Qual è il nome comune del corrispondente acido carbossilico a catena lineare?
Risposte
- acido esanoico
- acido valerale
Chiave Takeaways
- Gli acidi carbossilici semplici sono meglio conosciuti con nomi comuni basati su parole latine e greche che descrivono la loro fonte (es.g., acido formico, latino formica, che significa “formica”).
- Lettere greche, non numeri, designano la posizione degli acidi sostituiti nella convenzione comune di denominazione.
- I nomi IUPAC sono derivati dalla LCC dell’idrocarburo padre con la terminazione -e dell’alcano padre sostituita dal suffisso -oic e dalla parola acido.
Esercizi
-
Disegna la struttura di ogni composto.
- acido eptanoico
- acido 3-metilbutanoico
- acido 2,3-dibromobenzoico
- acidoβ-idrossibutirrico
-
Disegna la struttura di ogni composto.
- acido o-nitrobenzoico
- acido p-clorobenzoico
- acido 3-cloropentanoico
- acido α-cloropropionico
-
Nominare ogni composto con il nome IUPAC, il nome comune, o entrambi.
- (CH3)2CHCH2COOH
- (CH3)3CCH(CH3)CH2COOH
- CH2OHCH2CH2COOH
-
Nominare ogni composto col suo nome IUPAC.
- CH3(CH2)8COOH
- (CH3)2CHCCl2CH2CH2COOH
- CH3CHOHCH(CH2CH3)CHICOOH
Risposte
-
- CH3CH2CH2CH2CH2CH2COOH
-
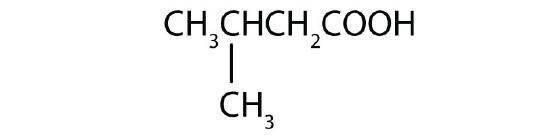
-
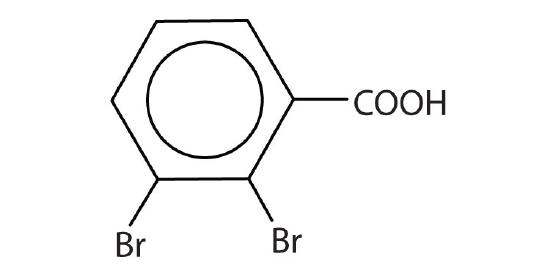
-
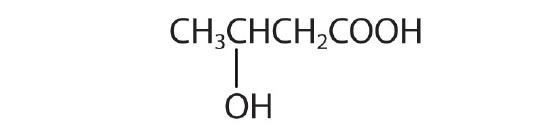
-
- 3-acido metilbutanoico; acido β-metilbutirrico
- 3,4,4-trimetilpentanoico
- 4- acido idrossibutanoico; acido γ-idrossibutirrico