Esercizio
1. Mostra come preparare il 3-metil2-pentanolo dal 3-metil-1-pentene.
Nota: Le domande 2-5 non hanno mostrato l’acqua presente nella soluzione di acido solforico e hanno indicato un secondo passo di neutralizzazione. Alcuni autori scrivono semplicemente H+/H2O come un singolo passo.
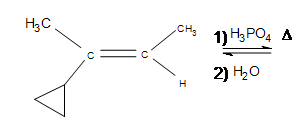
2. Disegna la struttura di legame per il prodotto.
.bmp?revision=1&size=bestfit&width=326&height=100)
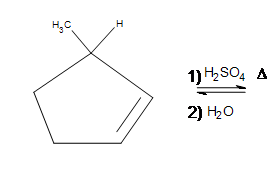
3. Disegna la struttura di legame per il prodotto. Come influisce il gruppo ciclopropano sulla reazione?
4. Disegna la struttura di legame del prodotto. (Suggerimento: cosa c’è di diverso in questo problema?)
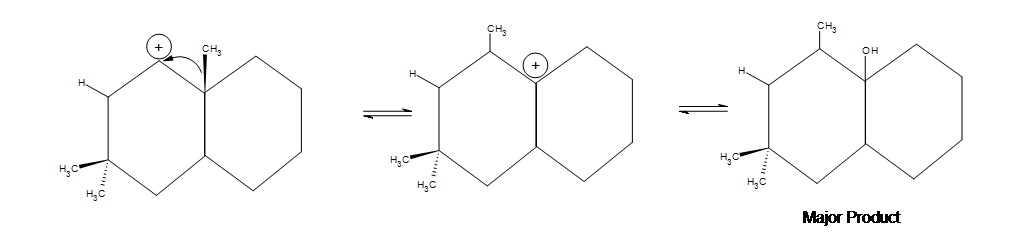
5. Disegna la struttura della linea di legame per il prodotto (o i prodotti). Indica eventuali spostamenti e il prodotto principale:

6. In ogni caso, predici il prodotto o i prodotti di questi reagenti di ossimerizzazione.

7. Proponi l’alchene che era il reagente per ognuno di questi prodotti di ossimercurazione.

Rispondi
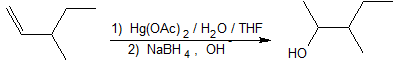
2. Questa reazione è una idratazione elettrofila.
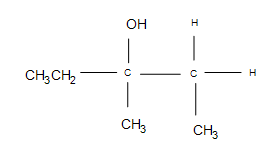
3. La risposta è prodotti collaterali aggiuntivi, ma il prodotto principale formato è sempre lo stesso (il prodotto mostrato). A seconda delle temperature utilizzate, il ciclopropano può aprirsi in una catena dritta, il che rende improbabile la formazione del prodotto principale (dopo la reazione, è improbabile che il 3º carbonio rimanga tale).
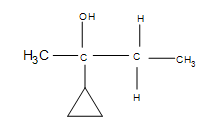
4. Uno spostamento di idruro si verifica effettivamente dalla cima dell’1-metilciclopentano a dove si era formato il carbocatione.
.bmp?revision=1&size=bestfit&width=290&height=201)
5. Nella prima immagine mostrata qui sotto, si verifica uno spostamento alchilico ma è possibile uno spostamento di idruro (che si verifica più velocemente). Perché non si verifica uno spostamento di idruro? La risposta è che lo spostamento alchilico porta a un prodotto più stabile. C’è una notevole quantità di prodotto laterale che si forma dove ci sono i due gruppi metilici, ma il prodotto principale mostrato qui sotto è ancora il più significativo a causa dell’iperconiugazione che avviene stando tra i due cicloesani.