Ejercicio
1. Muestre cómo preparar 3-metil2-pentanol a partir de 3-metil-1-penteno.
Nota: En las preguntas 2-5 no se ha mostrado el agua presente en la solución de ácido sulfúrico y se ha indicado un segundo paso de neutralización. Algunos autores simplemente escriben H+/H2O como un único paso.
2. Dibuje la estructura de la línea de enlace para el producto.
.bmp?revision=1&size=bestfit&width=326&height=100)
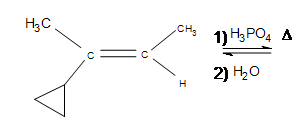
3. Dibuje la estructura de la línea de enlace para el producto. ¿Cómo afecta el grupo ciclopropano a la reacción?
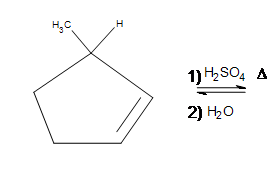
4. Dibuja la estructura de enlace del producto. (Pista: ¿Qué es diferente en este problema?)
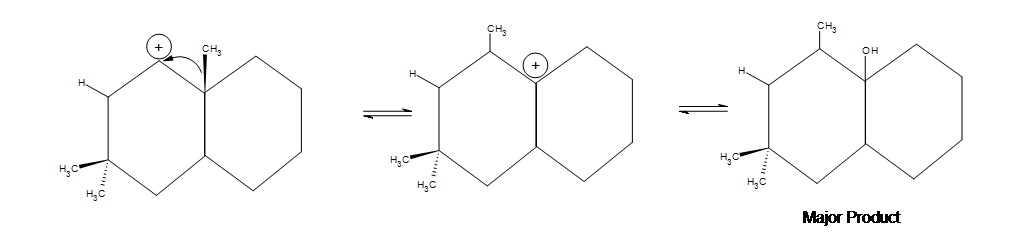
5. Dibuje la estructura de la línea de enlace para el (los) producto(s). Indique cualquier desplazamiento así como el producto principal:

6. En cada caso, prediga el producto o productos de estos reactivos de oximerización.

7. Proponga el alqueno que fue el reactante de cada uno de estos productos de oximerización.

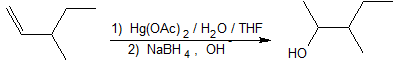
2. Esta reacción es una hidratación electrofílica.
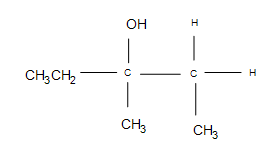
3. La respuesta es productos secundarios adicionales, pero el producto principal formado sigue siendo el mismo (el producto mostrado). Dependiendo de las temperaturas utilizadas, el ciclopropano puede abrirse en una cadena recta, lo que hace improbable que se forme el producto mayor (después de la reacción, es improbable que el 3º carbono permanezca como tal).
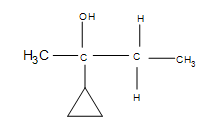
4. En realidad se produce un desplazamiento de hidruros desde la parte superior del 1-metilciclopentano hasta donde se había formado el carbocation.
.bmp?revision=1&size=bestfit&width=290&height=201)
5. En la primera imagen que se muestra a continuación, se produce un desplazamiento de alquilo pero es posible un desplazamiento de hidruro (que se produce más rápidamente). Por qué no se produce un desplazamiento de hidruro? La respuesta es porque el desplazamiento de alquilo conduce a un producto más estable. Hay una cantidad notable de producto secundario que se forma donde están los dos grupos metilo, pero el producto principal que se muestra a continuación sigue siendo el más significativo debido a la hiperconjugación que se produce al estar entre los dos ciclohexanos.