La servoventilación adaptativa (ASV) es una terapia ventilatoria no invasiva que proporciona una presión positiva inspiratoria variable en las vías respiratorias (IPAP) para apoyar la inspiración cuando la amplitud de la respiración se reduce, asegura una respiración suficiente cuando el esfuerzo respiratorio está ausente y proporciona una PAP fija o variable al final de la espiración (EPAP) para mantener la permeabilidad de las vías respiratorias superiores. Este enfoque está diseñado para imitar la PAP continua nasal (CPAP) en cuanto a la apertura neumática de las vías respiratorias superiores y para suprimir directamente las apneas centrales del sueño sin provocar una sobreventilación.1 En la apnea central del sueño (ACS) hipocápnica, en la que la hiperventilación desempeña un papel importante, se ha demostrado que la ASV aumenta ligeramente los niveles de dióxido de carbono en pacientes con insuficiencia cardíaca (IC).1
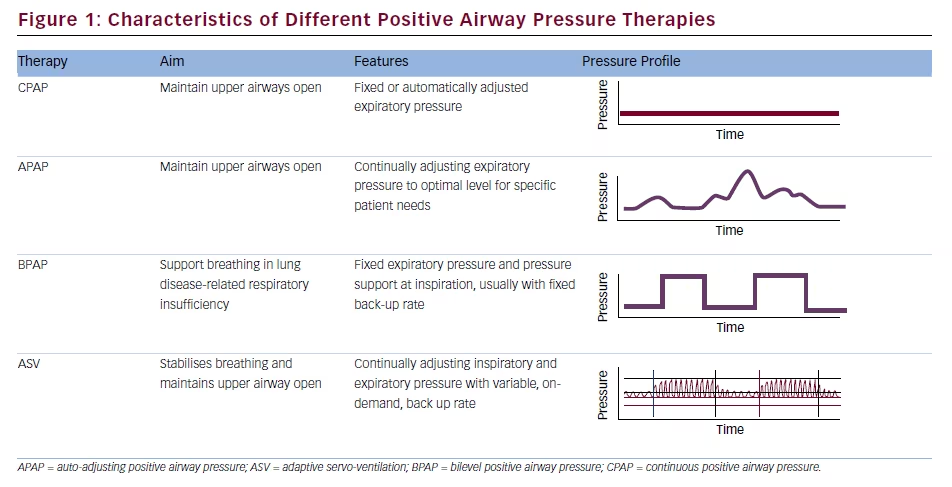
El perfil de presión proporcionado por los dispositivos de ASV difiere de los de otras terapias de PAP (véase la figura 1). Aunque se dispone de ajustes predeterminados, es más apropiada la titulación individualizada basada en el laboratorio del sueño para cada paciente,2 y el mejor enfoque para mantener la comodidad del paciente, maximizar la adherencia y preservar la hemodinámica es utilizar los ajustes mínimos efectivos para la IPAP, la EPAP y la tasa de respaldo.3
Últimos datos de ensayos sobre la servoventilación adaptativa
En general, los datos sobre el uso de los dispositivos ASV han procedido de estudios pequeños y/o no controlados y principalmente de clínicas del sueño. Esto ha cambiado recientemente con la publicación de los resultados del ensayo SERVE-HF.4
SERVE-HF fue el primer ensayo multicéntrico internacional de fase IV, aleatorizado y controlado a largo plazo, diseñado para investigar los efectos de la adición de ASV al tratamiento médico basado en las directrices, en comparación con el tratamiento médico solo (control), sobre la supervivencia y los resultados cardiovasculares en pacientes con IC sintomática y fracción de eyección (FE) reducida (HFrEF; FE ≤45 %) que tenían CSA predominante. La capacidad del tratamiento con ASV para reducir significativamente el índice de apnea-hipopnea (IAH) y mejorar la saturación de oxígeno y otros parámetros de los trastornos respiratorios del sueño (SDB) se confirmó en SERVE-HF, pero estos efectos no se tradujeron en una mejora de los resultados clínicos4.
Inesperadamente, los resultados del ensayo fueron neutros para el criterio de valoración principal – primer evento del compuesto de muerte por cualquier causa, una intervención cardiovascular que salve la vida (definida como trasplante cardíaco,
implantación de un dispositivo de asistencia ventricular a largo plazo, la reanimación tras una parada cardiaca súbita o el choque adecuado para la arritmia ventricular en pacientes con un desfibrilador cardioversor implantado) o una hospitalización no planificada por empeoramiento de la IC – con una hazard ratio (HR) de 1.13 (intervalo de confianza del 95 %: 0,97; 1,32; p=0,113).4 Quizá lo más sorprendente fue la identificación de una señal de seguridad en el grupo de ASV, ya que los pacientes tratados con el dispositivo tenían un mayor riesgo de sufrir una muerte por todas las causas (HR 1,28; IC del 95 %: 1,06; 1,55; p=0,01) y cardiovascular (HR 1,34; IC del 95 %: 1,09; 1,65; p=0,006).4 No hubo diferencias significativas entre los grupos de ASV y de control con respecto a los síntomas, la capacidad de ejercicio o la calidad de vida. Los efectos de la ASV sobre los gases sanguíneos, la FE del ventrículo izquierdo y los biomarcadores se están evaluando en el subestudio principal SERVE-HF (NCT01164592),5 cuyos resultados estarán disponibles en breve. Dichos datos pueden ayudar a explicar mejor los principales hallazgos del SERVE-HF.
Aunque los resultados del SERVE-HF representan un cambio de paradigma para la ASV, sólo son aplicables a un subconjunto de pacientes tratados con ASV (es decir, aquellos con ICrEF y CSA predominante), y no hay ninguna evidencia que sugiera la necesidad de dejar de considerar este tratamiento por completo. La ASV se ha estudiado en otras indicaciones, y la evidencia acumulada sugiere que la ASV puede tener un papel en una serie de grupos de pacientes fuera de los que tienen ICFr.
Servoventilación adaptativa en la insuficiencia cardíaca con fracción de eyección conservada
Aunque el impacto pronóstico negativo de la IC con FE conservada (ICFp) es similar al de la ICFr,6 las dos formas de IC representan síndromes clínicos diferentes y, por tanto, deben estudiarse y tratarse por separado.7 La FEM de la IC es más frecuente en las mujeres y suele tener una etiología no isquémica6,8, y actualmente no existen tratamientos basados en la evidencia8. Además, existen importantes diferencias entre la ICFp y la ICFr con respecto a la gravedad y el alcance de la disfunción miocárdica, los patrones de remodelación de las cámaras del corazón y a nivel ultraestructural, y la respuesta a las intervenciones terapéuticas.7 Como resultado de estas diferencias, cabe esperar que los resultados durante el tratamiento con ASV en pacientes con ICFpEF sean diferentes de los de la población del estudio SERVE-HF que tenía ICFr.
Los resultados de dos estudios a pequeña escala9,10 con períodos de seguimiento de 12 y 18 meses, respectivamente, sugieren que los efectos beneficiosos de la ASV en pacientes con ICFpEF podrían ir más allá de las mejoras en el IAH y los parámetros del sueño. En un estudio, se comparó a los pacientes con ICF con respiración de Cheyne-Stokes (RSC) que fueron tratados con ASV (n=39) con pacientes similares que rechazaron la ASV por diversas razones (n=21) durante un seguimiento de 3 a 24 (media de 11,6) meses.9 Los resultados del estudio del sueño mostraron que la ASV redujo significativamente el IAH, la apnea e hipopnea más prolongadas y la desaturación máxima en comparación con los controles. Además, durante las pruebas de ejercicio cardiopulmonar, los pacientes del grupo de ASV frente al grupo de control presentaron aumentos significativos en el consumo máximo de oxígeno (valor absoluto y porcentaje previsto), el consumo de oxígeno en el umbral aeróbico-anaeróbico y el pulso de oxígeno. También se registraron disminuciones significativas en el diámetro de la aurícula izquierda y en la velocidad máxima de entrada mitral Doppler temprana (E)/velocidad máxima de entrada mitral Doppler auricular (A), además de aumentos significativos en A, la velocidad media de alargamiento diastólico temprano (e’) y E/e’.
En un estudio aleatorio que incluyó a 36 pacientes estables con ICFpEF con SDB central se comparó la tasa de eventos cardíacos entre los pacientes que recibieron tratamiento médico optimizado solo frente al tratamiento médico optimizado más ASV (seguimiento medio de 543 días). Un evento cardíaco se definió como muerte cardíaca o rehospitalización por descompensación de la IC. A lo largo de 6 meses de tratamiento, los pacientes con IC-FE en el grupo de ASV tuvieron una tasa de ausencia de eventos mayor (94,4%) que los del grupo sin ASV (61,1%; p10). También se documentaron mejoras significativamente mayores desde el inicio en los niveles de péptido natriurético tipo B y en la clase funcional de la Asociación Cardíaca de Nueva York (NYHA) en los grupos con ASV frente a los sin ASV, pero no hubo cambios significativos en la FE ventricular izquierda determinada ecocardiográficamente desde el inicio hasta los 6 meses. Desde el punto de vista del SDB, las reducciones desde el inicio del IAH fueron de 30,2/h en el grupo con ASV frente a 8.2/h en el grupo sin ASV (p10
Es posible que el aumento de la tasa de muerte súbita cardíaca asociada al tratamiento con ASV de la CSA en pacientes con ICFrEF identificado en SERVEHF4 pueda ser diferente en la ICFpEF, donde el riesgo subyacente de muerte súbita
Muerte cardíaca es menor. Sin embargo, se necesitan estudios más amplios a largo plazo con resultados clínicos concretos (por ejemplo, mortalidad) para responder definitivamente a esta pregunta. Hasta que se disponga de tales datos, la decisión sobre el uso de ASV para el tratamiento de la CSA en pacientes con IC-FEM debe tomarse de forma individualizada para cada paciente, con gestión por parte de un cardiólogo (véase más adelante la recomendación sobre el seguimiento del tratamiento con ASV).
Terapia de servoventilación adaptativa en la apnea del sueño
Apnea central del sueño emergente al tratamiento
La CSA emergente al tratamiento, anteriormente conocida como apnea del sueño compleja, se produce en aproximadamente el 5-15 % de los pacientes que se someten a la titulación de la PAP para la apnea obstructiva del sueño (AOS). La definición de apnea del sueño emergente es la persistencia o la aparición de apneas e hipopneas centrales durante el inicio del tratamiento con PAP sin una frecuencia respiratoria de apoyo para la AOS, a pesar de la resolución significativa de los eventos respiratorios obstructivos.11 En la mayoría de los pacientes, la apnea del sueño emergente es un fenómeno transitorio que no es estable a lo largo del tiempo.12-14 Una posible explicación es que la fragmentación del sueño y los cambios de fase del sueño asociados a la titulación de la CPAP provocan una inestabilidad del control ventilatorio. Esta sugerencia se ve respaldada por el hallazgo de que la ASV emergente al tratamiento se produce con mayor frecuencia en las noches en las que los pacientes tratados con CPAP duermen mal.12 Otros factores predisponentes podrían ser la presencia de enfermedad arterial coronaria, las apneas centrales preexistentes, la gravedad de la AOS y el uso de opiáceos.12,14 Sin embargo, se requiere tratamiento para el subgrupo de pacientes con ASV emergente al tratamiento que persiste durante el uso continuado de CPAP o PAP binivel (biPAP) sin una frecuencia de respaldo. En estos casos, la ASV es el tratamiento más adecuado.
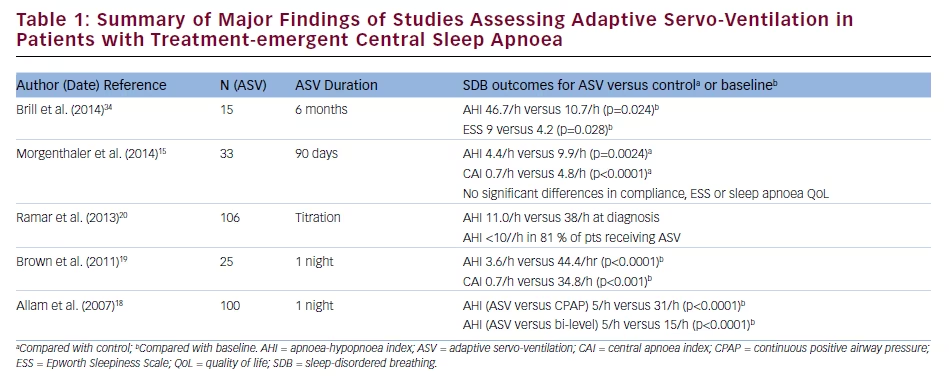
Los efectos de la ASV en los resultados clínicos y de la polisomnografía (PSG) en pacientes con CSA emergente al tratamiento se compararon con los de la CPAP en un ensayo clínico prospectivo y aleatorizado con 66 pacientes.15 Tras dos noches de titulación, el IAH fue de 5,7/h en el grupo de ASV frente a 14,1/h en el grupo de CPAP (p≤0,0003); los valores correspondientes tras 90 días de tratamiento fueron de 4,4/h y 9,9/h (p=0,0024). El IAC tras la titulación fue de 1,1/h con la ASV y de 8,8/h con la CPAP (p≤0,0003), y tras 90 días fue de 0,7/h frente a 4,8/h, respectivamente (p16 Los efectos beneficiosos de la ASV en un ensayo observacional prospectivo multicéntrico de 27 pacientes con ASI o ASI emergente al tratamiento incluyeron mejoras en el IAH, el IAC, el índice de apnea obstructiva y el índice de excitación durante la titulación del tratamiento, cambios que se mantuvieron durante 3 meses de tratamiento17. Además, hubo una reducción significativa en la puntuación de la Escala de Somnolencia de Epworth (ESS) durante la ASV (de 12,8 al inicio a 7,8; p=0,001); la adherencia media a la ASV fue de 4,2 h/noche. Estos datos están respaldados por los resultados de los análisis retrospectivos que demuestran que la ASV es más eficaz que otras terapias de PAP en lo que respecta a la reducción del IAH y la mejora de la calidad del sueño en los pacientes con CSA emergente del tratamiento.18-20 En la tabla 1 se presenta un resumen de los resultados de los estudios que investigan el uso de la ASV en pacientes con CSA emergente al tratamiento.
Respiración de Cheyne-Stokes inducida por opioides
Se han detectado apneas centrales mediante PSG en el 17-24 % de los pacientes que reciben tratamiento con opioides a largo plazo para el dolor crónico.21,22 Se ha demostrado que el tratamiento con ASV mejora el SDB en los consumidores de opiáceos en varios estudios clínicos, y el resultado de un metaanálisis mostró que el tratamiento con ASV en pacientes con CSA relacionada con los opiáceos dio lugar a que el 58 % de los pacientes alcanzaran un CAI de 23
Se observaron reducciones clínicamente significativas en el IAH, el CAI y el índice de hipopnea después de sólo 1 noche de uso de ASV en pacientes que recibían tratamiento con opiáceos a largo plazo para el dolor no maligno y que tenían CSA en un estudio multicéntrico prospectivo; Estas mejoras se mantuvieron a lo largo de 3 meses de tratamiento con ASV en casa.24 También se documentaron reducciones a corto y largo plazo en el IAH y el IAC durante el tratamiento con ASV en otro estudio sobre la ASC asociada a opiáceos, y el cumplimiento a largo plazo del tratamiento con ASV en este contexto fue bueno (media de 5,1 h/noche durante un período de seguimiento de 9 meses a 6 años).25 La proporción de respondedores también parece ser alta, con un 59,6% que logra un IAH de 26 La ASV también puede tener la capacidad de mejorar las apneas obstructivas en este contexto.27
Los datos comparativos muestran que la ASV es más eficaz para reducir las apneas centrales en los consumidores crónicos de opiáceos que la biPAP y la CPAP. En un pequeño grupo de receptores crónicos de opioides que no tuvieron ninguna mejora en la apnea del sueño durante 1 noche de tratamiento con CPAP, el uso de ASV durante 1 noche eliminó completamente las apneas centrales y obstructivas y redujo el índice de hipopnea a 13/h, en comparación con un IAH de 70/h al inicio y 55/h durante la CPAP28. En otro estudio, los valores del IAH y del IAC fueron significativamente
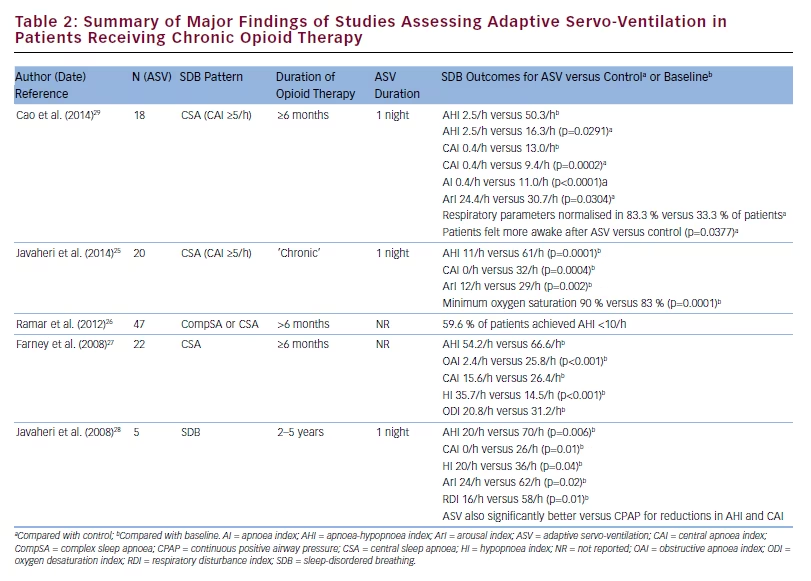
menores durante el uso a corto plazo de la ASV en comparación con la biPAP de modo espontáneo-temporizado (biPAP-ST) (2,5/h frente a 16.3/h; p=0,0005 y 0,4/h frente a 9,4/h; p=0,0002, respectivamente).29 En este ensayo prospectivo y cruzado, la proporción de pacientes que normalizaron sus parámetros respiratorios fue del 83,3 % durante la ASV y del 33.En este ensayo prospectivo y cruzado, la proporción de pacientes que normalizaron sus parámetros respiratorios fue del 83,3 % durante la ASV y del 33,3 % durante la bilevel-ST, y las puntuaciones del Cuestionario de Satisfacción del Paciente a la Mañana Siguiente mostraron que los pacientes se sentían más despiertos después de la ASV frente al tratamiento con bilevel-ST (p=0,0337).29 Los resultados de los estudios que investigan el uso de la ASV en pacientes con apnea del sueño que reciben un tratamiento a largo plazo con opioides se resumen en la Tabla 2.
Respiración de Cheyne-Stokes idiopática
En algunos casos, a pesar de las extensas investigaciones, no se encuentra ninguna causa obvia para la RSC-SC y esto se denomina RSC idiopática, cuya prevalencia exacta se desconoce. Se evaluó la viabilidad del uso de la ASV para tratar la RSC idiopática en tres pacientes que no habían respondido bien a la terapia de CPAP y oxígeno. El tratamiento con ASV redujo el índice de eventos anormales de 35,2/h a 3,5/h, y también hubo una reducción significativa del número de despertares (18,5/h a 1,1/h). Es importante destacar que el seguimiento a los 6-12 meses mostró una mejora significativa en el estado de alerta diurno y el estado de ánimo en los receptores de ASV.30
La apnea del sueño después de un ictus isquémico
El SDB puede documentarse en entre el 50 % y el 70 % de los pacientes después de un ictus isquémico agudo31,32 y persiste más allá del período agudo en una proporción sustancial de pacientes.33 Se investigó el papel de la ASV para el tratamiento de la ASC persistente tras un ictus isquémico agudo en 15 pacientes, 13 de los cuales habían sido tratados previamente sin éxito con CPAP o biPAP.34 El IAH era de 46,7/h al inicio, y disminuyó a 8,5/h (p=0,001) y 10,7/h (p=0,024) tras 3 y 6 meses de ASV, respectivamente. La ASV también mejoró la somnolencia diurna, con una disminución de la puntuación de la ESS de 8,6 al inicio a 5,6 durante la ASV (p=0,08). En los pacientes que utilizaron la ASV durante ≥5 h/noche, la puntuación de la ESS disminuyó de 9,0 al inicio a 4,2 (p=0,028). El uso de la ASV durante el ensayo fue bueno, con una media de 5 horas y 20 minutos por noche a los 3 meses y 6 horas y 22 minutos por noche a los 6 meses. La ASV también fue bien tolerada y no se notificaron efectos secundarios graves.
Cuándo no se debe utilizar la servoventilación adaptativa
Como siempre se ha hecho, la ASV no debe utilizarse en ninguna situación en la que haya hipoventilación en el estado basal. Por lo tanto, debe comprobarse la gasometría antes de iniciar el tratamiento, como para cualquier otra estrategia de ventilación. Además, basándose en los resultados del estudio SERVE-HF, la ASV está ahora contraindicada en pacientes con ICrEF (FE del ventrículo izquierdo del 45 % o menos) y CSA predominante. Todos los receptores actuales de ASV que cumplan estos criterios deben ser informados de los resultados del estudio SERVE-HF y de sus implicaciones, y cambiar a un modo de tratamiento alternativo.
Terapia de monitorización
Actualmente no existen directrices publicadas sobre la monitorización y el seguimiento de los pacientes durante el tratamiento con ASV. Por lo tanto, los médicos deben utilizar su experiencia en la práctica clínica y el sentido común. Antes de iniciar el tratamiento, parece apropiado comprobar si hay síntomas de IC, revisar cuidadosamente la historia clínica del paciente (prestando especial atención a los eventos cardíacos) y, en caso de duda, determinar la FE del ventrículo izquierdo mediante ecocardiografía (especialmente en pacientes que puedan tener una enfermedad cardiovascular). El seguimiento a corto plazo debe incluir la comprobación de las fugas, los efectos secundarios y la adherencia al tratamiento. La evaluación de la eficacia del tratamiento con poligrafía o PSG después de 1 a 3 meses, y un seguimiento a los 6 meses consistente en una entrevista clínica, descarga de la máquina y evaluación clínica completa parece razonable. La monitorización ecocardiográfica continua de la FE parece prudente cuando se utiliza ASV en pacientes con enfermedad cardíaca.
Perspectiva y direcciones futuras
Un área importante de investigación en curso es dilucidar los mecanismos fisiopatológicos que subyacen a la señal de seguridad cardiovascular identificada en los pacientes con ICrEF tratados con ASV en el estudio SERVE-HF. Esto permitirá identificar subgrupos específicos de pacientes con ICFrEF en los que debería evitarse la ASV, y otros que podrían beneficiarse del tratamiento con ASV. Se espera que los datos del subestudio principal SERVE-HF5 y el análisis durante el tratamiento, el ensayo ADVENT-HF (NCT01128816) y los registros en curso, como el estudio de cohortes prospectivo y multicéntrico francés FACE35 , proporcionen alguna información sobre el uso de la ASV en subgrupos de pacientes con ICFr con CSA, pacientes con ICFr y AOS o AOS con CSA coexistente y aquellos con ICFpEF y ambas formas de SDB. Los efectos de la ASV en pacientes con IC descompensada aguda se están investigando en el estudio CAT-HF (NCT01953874). Fuera de la IC, se necesitan más datos sobre el uso de ASV en pacientes con diferentes fenotipos de CSA, incluidas las apneas centrales emergentes por tratamiento y las inducidas por opioides.
Conclusión
Existen varias preguntas sin respuesta sobre el lugar actual y futuro del tratamiento con ASV en pacientes con diversas formas de SDB. Según los resultados del estudio SERVE-HF, el tratamiento con ASV debe evitarse en pacientes con ICrEF y CSA predominante con RSC, y cuando se utiliza ASV en otras indicaciones se recomienda una estrecha vigilancia del paciente, especialmente en los subgrupos con riesgo de desarrollar IC. Sin embargo, los datos actualmente disponibles sugieren que la ASV tiene efectos beneficiosos en pacientes con ASI emergente, apneas centrales asociadas a la terapia con opioides a largo plazo sin hipoventilación alveolar, RSC idiopática, después de un accidente cerebrovascular isquémico y en aquellos con IC-FEp. Todavía no se dispone de datos a largo plazo sobre los efectos de la ASV en la morbilidad y la mortalidad en estos grupos de pacientes y, por lo tanto, el inicio del tratamiento es una decisión que debe tomarse individualmente para cada paciente, y la terapia debe continuarse sólo si el paciente muestra mejoras subjetivas y objetivas durante el tratamiento.
ADVENT-HF = El efecto de la servoventilación adaptativa sobre la supervivencia y los ingresos hospitalarios en la insuficiencia cardíaca
CAT-HF = Mejoras cardiovasculares con la terapia de ASV MV en la insuficiencia cardíaca
FACE = Estudio de cohorte francés de pacientes con insuficiencia cardíaca crónica con apnea central del sueño elegibles para servoventilación adaptativa
.Ventilación Adaptativa
SERVE-HF = Tratamiento de los Trastornos Respiratorios del Sueño con Apnea Central del Sueño Predominante mediante Servoventilación Adaptativa en Pacientes con Insuficiencia Cardíaca