Cele nauczania
Po ukończeniu tej sekcji, powinieneś być w stanie
-
- zapisać równanie reprezentujące powstawanie mydła.
- zidentyfikować strukturę tłuszczu wymaganą do produkcji danego mydła.
- zidentyfikować strukturę mydła, biorąc pod uwagę strukturę tłuszczu, z którego jest produkowane.
- opisać mechanizm, dzięki któremu mydła wywierają swoje działanie oczyszczające.
- podać chemiczne wyjaśnienie problemów napotykanych, gdy mydła karboksylanowe są stosowane w obszarach o twardej wodzie i wyjaśnić, jak można je przezwyciężyć poprzez zastosowanie detergentów sulfonianowych.
Kluczowe pojęcia
Upewnij się, że potrafisz zdefiniować i zastosować w kontekście poniższe kluczowe pojęcia.
- hydrofilowe
- lipofilowe (hydrofobowe)
- amfifilowe
- mikrocząsteczki
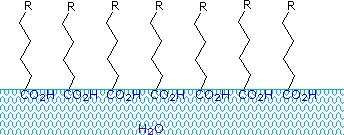
Kwasy karboksylowe i sole posiadające łańcuchy alkilowe dłuższe niż osiem węgli wykazują niezwykłe zachowanie w wodzie ze względu na obecność zarówno regionów hydrofilowych (CO2), jak i hydrofobowych (alkilowych) w tej samej cząsteczce. Takie cząsteczki są określane jako amfifilowe (Gk. amphi = oba) lub amfipatyczne. Kwasy tłuszczowe składające się z dziesięciu lub więcej atomów węgla są prawie nierozpuszczalne w wodzie, a z powodu ich mniejszej gęstości, po zmieszaniu z wodą unoszą się na powierzchni. W przeciwieństwie do parafiny lub innych alkanów, które mają tendencję do tworzenia kałuż na powierzchni wody, te kwasy tłuszczowe rozprzestrzeniają się równomiernie na rozszerzonej powierzchni wody, tworząc w końcu monomolekularną warstwę, w której polarne grupy karboksylowe są związane wodorem na granicy wody, a łańcuchy węglowodorowe są wyrównane razem z dala od wody. Zachowanie to ilustruje diagram po prawej stronie. Substancje, które gromadzą się na powierzchni wody i zmieniają jej właściwości, nazywane są surfaktantami.
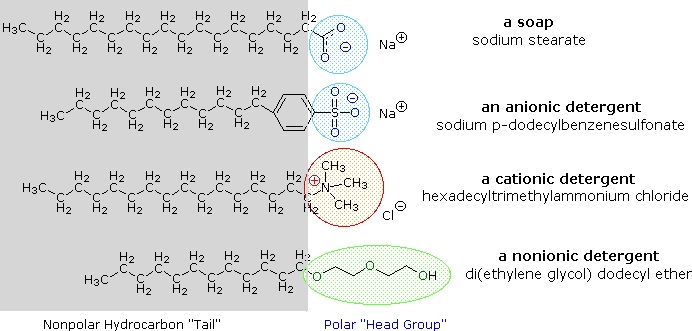
Sole metali alkalicznych kwasów tłuszczowych są bardziej rozpuszczalne w wodzie niż same kwasy, a amfifilowy charakter tych substancji sprawia, że są one również silnymi surfaktantami. Najbardziej powszechnymi przykładami takich związków są mydła i detergenty, z których cztery przedstawiono poniżej. Zauważ, że każda z tych cząsteczek ma niepolarny łańcuch węglowodorowy, „ogon”, i polarną (często jonową) „grupę główną”. Zastosowanie takich związków jako środków czyszczących jest ułatwione dzięki ich powierzchniowo czynnemu charakterowi, który obniża napięcie powierzchniowe wody, umożliwiając jej penetrację i zwilżanie różnych materiałów.
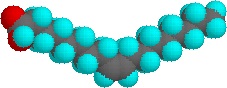
Niewielkie ilości tych środków powierzchniowo czynnych rozpuszczają się w wodzie, dając losowe rozproszenie cząsteczek solutu. Jednakże, gdy stężenie jest zwiększane, zachodzi interesująca zmiana. Cząsteczki surfaktantów w sposób odwracalny łączą się w polimolekularne agregaty zwane micelami. Dzięki skupieniu łańcuchów hydrofobowych w centrum miceli, zaburzenie struktury wiązań wodorowych w ciekłej wodzie jest zminimalizowane, a polarne grupy główne rozciągają się na otaczającą wodę, gdzie uczestniczą w wiązaniach wodorowych. Takie micele mają często kształt kulisty, ale mogą też przyjmować formy cylindryczne i rozgałęzione, jak pokazano po prawej stronie. Tutaj polarna grupa głowowa jest oznaczona niebieskim kółkiem, a niepolarny ogon czarną zygzakowatą linią.
Najstarszym amfifilowym środkiem czyszczącym znanym człowiekowi jest mydło. Mydło jest wytwarzane w procesie katalizowanej przez zasadę hydrolizy (zmydlania) tłuszczu zwierzęcego (patrz poniżej). Zanim wodorotlenek sodu stał się dostępny w handlu, używano wrzącego roztworu węglanu potasu wyługowanego z popiołów drzewnych. Miękkie mydła potasowe były następnie przekształcane w twardsze mydła sodowe poprzez mycie roztworem soli. Znaczenie mydła dla cywilizacji ludzkiej jest udokumentowane historycznie, ale dostrzeżono pewne problemy związane z jego używaniem. Jeden z nich spowodowany jest słabą kwasowością (pKa ok. 4,9) kwasów tłuszczowych. Roztwory mydeł metali alkalicznych są lekko alkaliczne (pH 8 do 9) z powodu hydrolizy. Jeśli pH roztworu mydła zostanie obniżone przez kwaśne zanieczyszczenia, nierozpuszczalne kwasy tłuszczowe wytrącają się i tworzą szumowiny. Drugi problem jest spowodowany obecnością soli wapnia i magnezu w dostarczanej wodzie (twarda woda). Te dwuwartościowe kationy powodują agregację miceli, które następnie osadzają się jako brudna szumowina.
Problemy te zostały złagodzone dzięki opracowaniu syntetycznych amfifili zwanych detergentami (lub syndetami). Dzięki zastosowaniu znacznie silniejszego kwasu jako polarnej grupy głównej, wodne roztwory amfifili są mniej wrażliwe na zmiany pH. Również funkcje sulfonianowe stosowane w praktycznie wszystkich detergentach anionowych nadają większą rozpuszczalność micelom zawierającym kationy ziem alkalicznych występujących w twardej wodzie. Wariacje na temat amfifilów doprowadziły do powstania innych klas, takich jak detergenty kationowe i niejonowe przedstawione powyżej. Detergenty kationowe często wykazują właściwości bakteriobójcze, a ich zdolność do zmiany pH powierzchni sprawiła, że są przydatne jako zmiękczacze tkanin i odżywki do włosów. Te wszechstronne „narzędzia” chemiczne w ciągu ostatnich pięćdziesięciu lat radykalnie zmieniły rynki środków czyszczących do użytku domowego i osobistego
Reakcje chemiczne tłuszczów i olejów
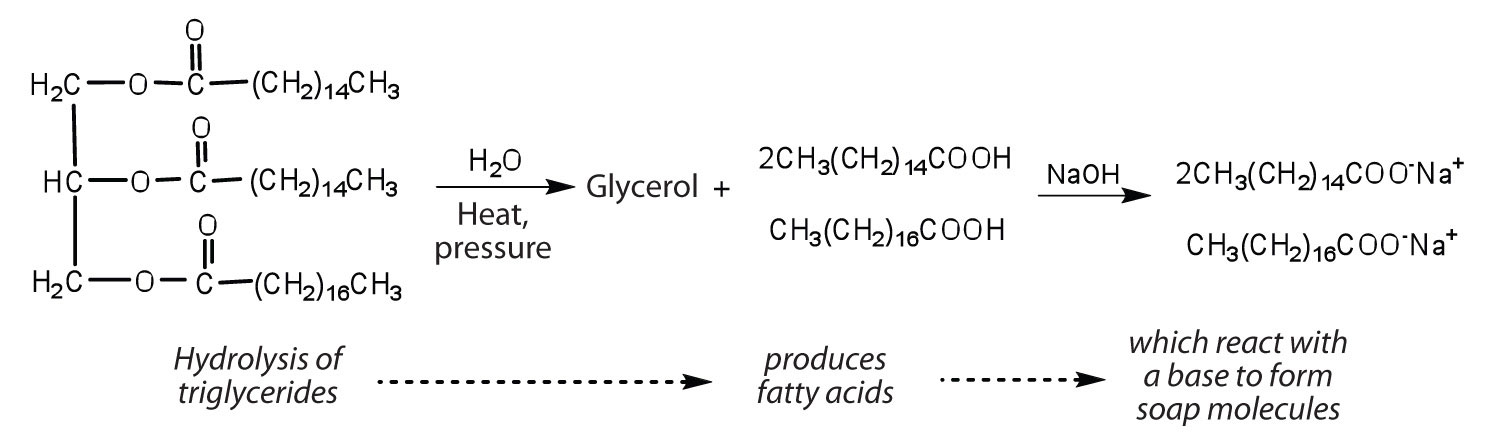
Tłuszcze i oleje mogą uczestniczyć w wielu reakcjach chemicznych – na przykład, ponieważ trójglicerydy są estrami, mogą być hydrolizowane w obecności kwasu, zasady lub specyficznych enzymów znanych jako lipazy. Hydroliza tłuszczów i olejów w obecności zasady jest wykorzystywana do produkcji mydła i nazywana jest zmydlaniem. Obecnie większość mydeł jest przygotowywana poprzez hydrolizę triglicerydów (często z łoju, oleju kokosowego lub obu) przy użyciu wody pod wysokim ciśnieniem i w wysokiej temperaturze. Węglan sodu lub wodorotlenek sodu jest następnie stosowany do przekształcania kwasów tłuszczowych w ich sole sodowe (cząsteczki mydła):
Wydawcy i przypisy
-
Dr. Dietmar Kennepohl FCIC (profesor chemii, Uniwersytet Athabasca)
-
Prof. Steven Farmer (Sonoma State University)
-
William Reusch, Professor Emeritus (Michigan State U.), Virtual Textbook of Organic Chemistry
- The Basics of General, Organic, and Biological Chemistry by David W. Ball, John W. Hill, and Rhonda J. Scott.