La servoventilazione adattiva (ASV) è una terapia ventilatoria non invasiva che fornisce una pressione positiva delle vie aeree inspiratorie (IPAP) variabile per sostenere l’ispirazione quando l’ampiezza del respiro è ridotta, assicura una respirazione sufficiente quando lo sforzo respiratorio è assente e fornisce una PAP end-espiratoria (EPAP) fissa o variabile per mantenere la pervietà delle vie aeree superiori. Questo approccio è stato progettato per imitare la PAP nasale continua (CPAP) in termini di apertura pneumatica delle vie aeree superiori e per sopprimere direttamente le apnee notturne centrali senza causare una sovraventilazione.1 Nelle apnee notturne centrali ipocapniche (CSA), in cui l’iperventilazione gioca un ruolo fondamentale, l’ASV ha dimostrato di aumentare leggermente i livelli di anidride carbonica nei pazienti con insufficienza cardiaca (HF).1
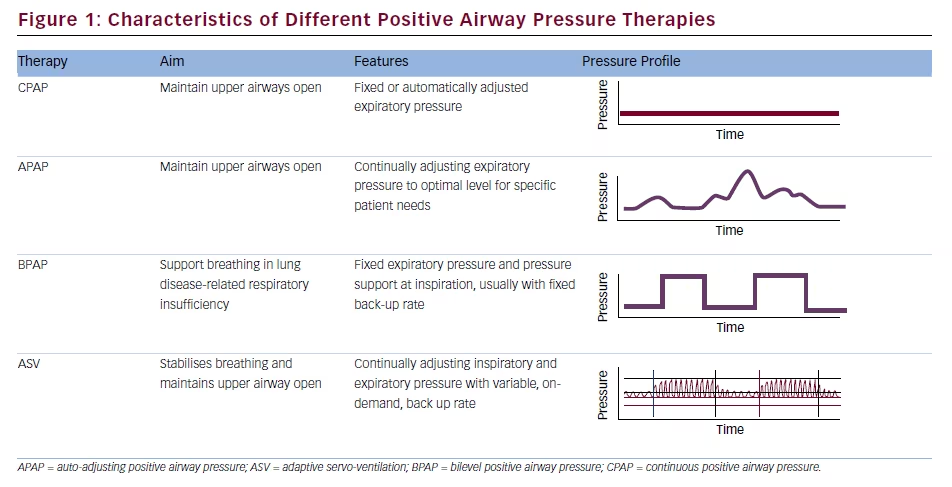
Il profilo di pressione fornito dai dispositivi ASV differisce da quello di altre terapie PAP (vedi Figura 1). Sebbene siano disponibili impostazioni predefinite, la titolazione individualizzata per ogni paziente basata sul laboratorio del sonno è più appropriata,2 e l’approccio migliore per mantenere il comfort del paziente, massimizzare l’aderenza e preservare l’emodinamica è quello di utilizzare le impostazioni minime efficaci per IPAP, EPAP e tasso di back-up.3
I più recenti dati degli studi sulla servoventilazione adattiva
In generale, i dati sull’uso dei dispositivi ASV provengono da studi piccoli e/o non controllati e principalmente da cliniche del sonno. Questo è cambiato recentemente con la pubblicazione dei risultati dello studio SERVE-HF.4
SERVE-HF è stato il primo studio internazionale multicentrico di fase IV, randomizzato e controllato a lungo termine, progettato per studiare gli effetti dell’aggiunta di ASV alla gestione medica basata sulle linee guida rispetto alla sola gestione medica (controllo) sulla sopravvivenza e sugli esiti cardiovascolari nei pazienti con HF sintomatica e ridotta frazione di eiezione (EF) (HFrEF; EF ≤45 %) che avevano CSA predominante. La capacità della terapia ASV di ridurre significativamente l’indice di apnea-ipopnea (AHI) e di migliorare la saturazione di ossigeno e altri parametri della respirazione disturbata dal sonno (SDB) è stata confermata nel SERVE-HF, ma questi effetti non si sono tradotti in migliori risultati clinici.4
Inaspettatamente, i risultati dello studio sono stati neutrali per l’endpoint primario – primo evento del composito di morte per qualsiasi causa, un intervento cardiovascolare salvavita (definito come trapianto cardiaco,
impianto di un dispositivo di assistenza ventricolare a lungo termine, rianimazione dopo arresto cardiaco improvviso o shock appropriato per aritmia ventricolare in pazienti con defibrillatore cardioverter impiantato) o un ricovero non pianificato per peggioramento della HF – con un hazard ratio (HR) di 1.13 (intervallo di confidenza al 95% 0,97, 1,32; p=0,113).4 Forse ancora più sorprendente è stata l’identificazione di un segnale di sicurezza nel gruppo ASV, con i pazienti trattati con il dispositivo a più alto rischio di andare incontro a morte per tutte le cause (HR 1,28, 95% CI 1,06, 1,55; p=0,01) e cardiovascolare (HR 1,34, 95% CI 1,09, 1,65; p=0,006).4 Non ci sono state differenze significative tra il gruppo ASV e il gruppo di controllo per quanto riguarda i sintomi, la capacità di esercizio o la qualità della vita. Gli effetti dell’ASV su gas sanguigni, EF ventricolare sinistro e biomarcatori sono in corso di valutazione nel SERVE-HF major substudy (NCT01164592),5 i cui risultati saranno presto disponibili. Tali dati possono contribuire a spiegare meglio i principali risultati del SERVE-HF.
Anche se i risultati del SERVE-HF rappresentano un cambiamento di paradigma per l’ASV, sono applicabili solo a un sottoinsieme di pazienti trattati con ASV (cioè quelli con HFrEF e CSA predominante), e non ci sono prove che suggeriscano la necessità di smettere di considerare questa terapia. L’ASV è stata studiata in altre indicazioni e le prove che si stanno accumulando suggeriscono che l’ASV può avere un ruolo in un certo numero di gruppi di pazienti al di fuori di quelli con HFrEF.
La servoventilazione adattativa nell’insufficienza cardiaca con frazione di eiezione conservata
Anche se l’impatto prognostico negativo della HF con EF conservata (HFpEF) è simile a quello della HFrEF,6 le due forme di HF rappresentano sindromi cliniche diverse e quindi dovrebbero essere studiate e trattate separatamente.7 L’HFpEF è più comune nelle donne e più spesso ha un’eziologia nonishaemica,6,8 e attualmente non sono disponibili trattamenti basati sull’evidenza.8 Inoltre, esistono importanti differenze tra l’HFpEF e l’HFrEF per quanto riguarda l’acutezza e l’estensione della disfunzione miocardica, i modelli di rimodellamento nelle camere cardiache e a livello ultrastrutturale e la risposta agli interventi terapeutici.7 Come risultato di queste differenze, i risultati durante la terapia con ASV nei pazienti con HFpEF dovrebbero essere diversi da quelli della popolazione dello studio SERVE-HF che aveva HFrEF.
I risultati di due studi su piccola scala9,10 con periodi di follow-up di 12 e 18 mesi, rispettivamente, suggeriscono che gli effetti benefici dell’ASV nei pazienti con HFpEF potrebbero estendersi oltre il miglioramento dell’AHI e dei parametri del sonno. In uno studio, i pazienti con HFpEF con respirazione di Cheyne-Stokes (RSI) che sono stati trattati con ASV (n=39) sono stati confrontati con pazienti simili che hanno rifiutato l’ASV per vari motivi (n=21) per un follow-up di 3-24 (media 11,6) mesi.9 I risultati dello studio del sonno hanno mostrato che l’ASV ha ridotto significativamente l’AHI, le apnee e le ipopnee più lunghe e la desaturazione massima rispetto ai controlli. Inoltre, durante il test da sforzo cardiopolmonare, i pazienti nel gruppo ASV rispetto al gruppo di controllo hanno avuto aumenti significativi nel picco di assorbimento di ossigeno (valore assoluto e percentuale prevista), assorbimento di ossigeno alla soglia aerobica-anaerobica e impulso di ossigeno. Sono state riportate anche diminuzioni significative del diametro atriale sinistro e della velocità di picco dell’afflusso mitrale Doppler precoce (E)/velocità di picco dell’afflusso mitrale Doppler atriale (A), oltre ad aumenti significativi di A, della velocità media di allungamento diastolico precoce (e’) e di E/e’.
In uno studio randomizzato che includeva 36 pazienti HFpEF stabili con SDB centrale, il tasso di eventi cardiaci è stato confrontato tra i pazienti che hanno ricevuto il solo trattamento medico ottimizzato rispetto al trattamento medico ottimizzato più ASV (follow-up medio 543 giorni). Un evento cardiaco è stato definito come morte cardiaca o riospedalizzazione per scompenso dell’HF. Nel corso di 6 mesi di trattamento, i pazienti con HFpEF nel gruppo ASV hanno avuto un tasso di assenza di eventi (94,4 %) superiore a quelli nel gruppo senza ASV (61,1 %; p10 Miglioramenti significativamente maggiori dal basale sono stati documentati anche nei livelli di peptide natriuretico di tipo B e nella classe funzionale della New York Heart Association (NYHA) nei gruppi ASV rispetto a quelli senza ASV, ma non vi è stato alcun cambiamento significativo nell’EF ventricolare sinistro determinato ecocardiograficamente dal basale ai 6 mesi. Da una prospettiva SDB, le riduzioni dal basale nell’AHI erano 30.2/h nel gruppo ASV contro 8.2/h nel gruppo senza ASV (p10
È possibile che l’aumento del tasso di morte cardiaca improvvisa associato al trattamento ASV del CSA nei pazienti con HFrEF identificato nel SERVEHF4 possa essere diverso nell’HFpEF, dove il rischio sottostante di morte cardiaca improvvisa
cardiac death è inferiore. Tuttavia, per rispondere definitivamente a questa domanda sono necessari studi a lungo termine più ampi con risultati clinici concreti (ad esempio la mortalità). Fino a quando tali dati non saranno disponibili, la decisione di usare o meno l’ASV per il trattamento della CSA nei pazienti con HFpEF deve essere presa su base individuale, con la gestione di un cardiologo (vedi sotto per la raccomandazione sul monitoraggio della terapia ASV).
Terapia di servoventilazione adattiva nell’apnea notturna
Apnea notturna centrale emergente dal trattamento
La CSA emergente dal trattamento, precedentemente nota come apnea notturna complessa, si verifica in circa il 5-15% dei pazienti che si sottopongono alla titolazione della PAP per l’apnea ostruttiva del sonno (OSA). La definizione di CSA emergente al trattamento è la persistenza o l’emergere di apnee centrali e ipopnee durante l’inizio della terapia PAP senza una frequenza respiratoria di riserva per l’OSA, nonostante la risoluzione significativa degli eventi respiratori ostruttivi.11 Per la maggior parte dei pazienti, la CSA emergente al trattamento è un fenomeno transitorio che non è stabile nel tempo.12-14 Una possibile spiegazione è che la frammentazione del sonno e gli spostamenti di fase del sonno associati alla titolazione della CPAP causano instabilità del controllo ventilatorio. Questo suggerimento è supportato dalla scoperta che la CSA da trattamento si verifica più frequentemente nelle notti in cui i pazienti trattati con CPAP dormono male.12 Altri fattori predisponenti potrebbero essere la presenza di malattia coronarica, le apnee centrali preesistenti, la gravità dell’OSA e l’uso di oppioidi.12,14 Tuttavia, il trattamento è necessario per il sottogruppo di pazienti con CSA da trattamento che persiste durante l’uso continuato di CPAP o PAP bilevel (biPAP) senza una frequenza di riserva. In tali contesti, l’ASV è la terapia più appropriata.
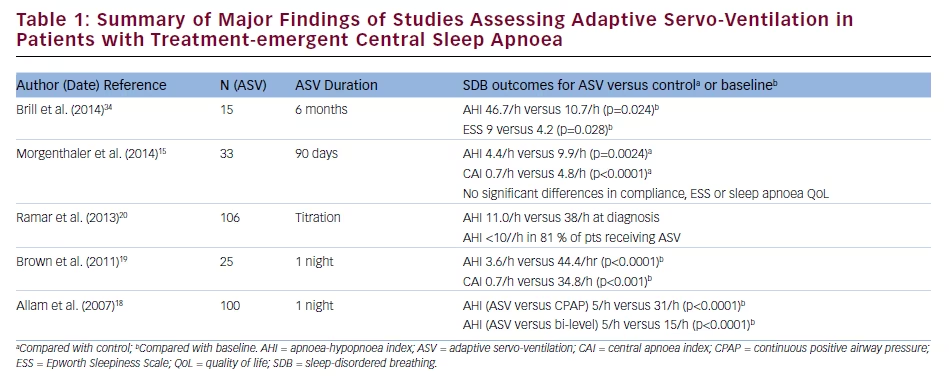
Gli effetti dell’ASV sui risultati clinici e della polisonnografia (PSG) nei pazienti con CSA emergente dal trattamento sono stati confrontati con quelli della CPAP in uno studio clinico prospettico e randomizzato su 66 pazienti.15 Dopo due notti di titolazione, l’AHI era di 5,7/h nel gruppo ASV contro 14,1/h nel gruppo CPAP (p≤0,0003); i valori corrispondenti dopo 90 giorni di trattamento erano 4,4/h e 9,9/h (p=0,0024). Il CAI dopo la titolazione era 1,1/h con ASV e 8,8/h con CPAP (p≤0,0003), e dopo 90 giorni era 0,7/h contro 4,8/h, rispettivamente (p16 Gli effetti benefici dell’ASV in uno studio osservazionale prospettico multicentrico su 27 pazienti con CSA o CSA emergente dal trattamento includevano miglioramenti nell’AHI, CAI, indice di apnea ostruttiva e indice di eccitazione durante la titolazione della terapia, cambiamenti che sono stati mantenuti per 3 mesi di trattamento.17 Inoltre, c’è stata una riduzione significativa del punteggio della Epworth Sleepiness Scale (ESS) durante l’ASV (da 12,8 al basale a 7,8; p=0,001); l’aderenza media all’ASV è stata di 4,2 h/notte. Questi dati sono supportati dai risultati di analisi retrospettive che dimostrano che l’ASV è più efficace di altre terapie PAP per quanto riguarda la riduzione dell’AHI e il miglioramento della qualità del sonno nei pazienti con CSA emergente dal trattamento.18-20 Un riassunto dei risultati degli studi che indagano l’uso dell’ASV in pazienti con CSA emergente dal trattamento è presentato nella tabella 1.
Respirazione di Cheyne-Stokes indotta da oppioidi
Le apnee centrali sono state rilevate utilizzando la PSG nel 17-24% dei pazienti sottoposti a terapia a lungo termine con oppioidi per il dolore cronico.21,22 La terapia con ASV ha dimostrato di migliorare la SDB nei consumatori di oppioidi in una serie di studi clinici, e il risultato di una meta-analisi ha dimostrato che il trattamento con ASV in pazienti con CSA correlata agli oppioidi ha portato il 58% dei pazienti a raggiungere un CAI di 23
Riduzioni clinicamente significative dell’AHI, del CAI e dell’indice di ipopnea sono state osservate dopo solo 1 notte di utilizzo dell’ASV in pazienti in terapia a lungo termine con oppioidi per dolore non maligno che avevano CSA in uno studio prospettico multicentrico; Questi miglioramenti sono stati mantenuti per 3 mesi di terapia ASV domiciliare.24 Riduzioni sia a breve che a lungo termine dell’AHI e del CAI durante la terapia con ASV sono state documentate anche in un altro studio sulla CSA associata agli oppioidi, e l’aderenza a lungo termine alla terapia con ASV in questo contesto è stata buona (media di 5,1 h/notte in un periodo di follow-up da 9 mesi a 6 anni).25 Anche la percentuale di pazienti che rispondono sembra essere alta, con il 59,6% che raggiunge un AHI di 26 L’ASV può anche avere la capacità di migliorare le apnee ostruttive in questo contesto.27
I dati comparativi mostrano che l’ASV è più efficace nel ridurre le apnee centrali nei consumatori cronici di oppioidi rispetto alla biPAP e alla CPAP. In un piccolo gruppo di consumatori cronici di oppioidi che non hanno avuto alcun miglioramento dell’apnea notturna durante 1 notte di terapia con CPAP, l’uso dell’ASV per 1 notte ha eliminato completamente le apnee centrali e ostruttive e ha ridotto l’indice di ipopnea a 13/h, rispetto a un AHI di 70/h al basale e 55/h durante la CPAP.28 In un altro studio, i valori di AHI e CAI erano significativamente
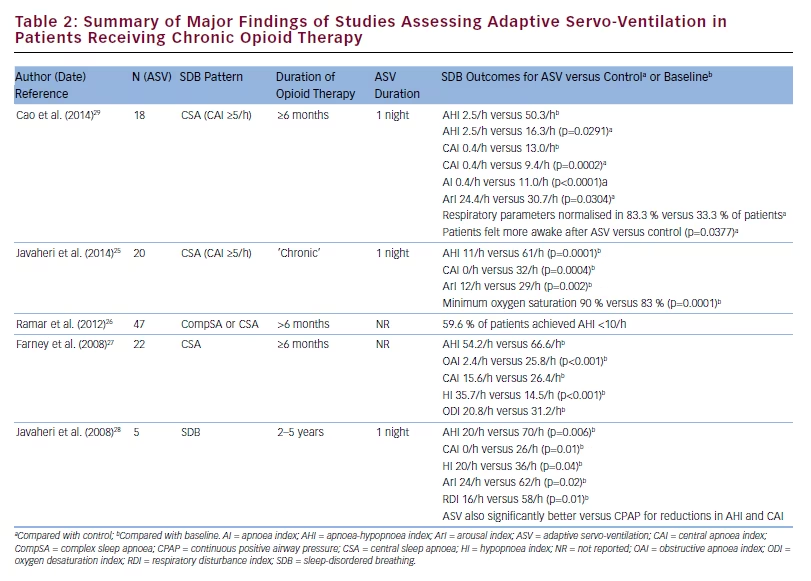
più bassi durante l’uso a breve termine dell’ASV rispetto alla biPAP in modalità spontanea (biPAP-ST) (2,5/h contro 16.3/h; p=0,0005 e 0,4/h contro 9,4/h; p=0,0002, rispettivamente).29 In questo studio prospettico e crossover, la proporzione di pazienti che avevano parametri respiratori normalizzati era dell’83,3% durante l’ASV e del 33,3% durante la biPAP-ST.3 % durante la bilevel-ST, e i punteggi del Morning After Patient Satisfaction Questionnaire hanno mostrato che i pazienti si sentivano più svegli dopo l’ASV rispetto al trattamento con bilevel-ST (p=0,0337).29 I risultati degli studi che indagano l’uso dell’ASV in pazienti con apnea notturna che ricevono una terapia a lungo termine con oppioidi sono riassunti nella tabella 2.
Respirazione idiopatica di Cheyne-Stokes
In alcuni casi, nonostante indagini approfondite, non viene trovata alcuna causa evidente per la CSA-CSR e si parla di RSI idiopatica, la cui esatta prevalenza è sconosciuta. La fattibilità dell’uso di ASV per trattare la RSI idiopatica è stata valutata in tre pazienti che non avevano risposto bene alla CPAP e all’ossigenoterapia. Il trattamento con ASV ha ridotto l’indice degli eventi anomali da 35,2/h a 3,5/h, e c’è stata anche una riduzione significativa del numero di risvegli (da 18,5/h a 1,1/h). È importante notare che il follow-up a 6-12 mesi ha mostrato un miglioramento significativo della vigilanza diurna e dell’umore nei destinatari dell’ASV.30
L’apnea notturna dopo l’ictus ischemico
L’ASV può essere documentata in una percentuale compresa tra il 50% e il 70% dei pazienti dopo un ictus ischemico acuto31,32 e persiste oltre il periodo acuto in una percentuale sostanziale di pazienti.33 Il ruolo dell’ASV per il trattamento della CSA persistente dopo l’ictus ischemico acuto è stato studiato in 15 pazienti, 13 dei quali erano stati precedentemente trattati senza successo con CPAP o biPAP.34 L’AHI era 46,7/h al basale, ed è diminuito a 8,5/h (p=0,001) e 10,7/h (p=0,024) dopo 3 e 6 mesi di ASV, rispettivamente. L’ASV ha anche migliorato la sonnolenza diurna, con una diminuzione del punteggio ESS da 8,6 al basale a 5,6 durante l’ASV (p=0,08). Nei pazienti che hanno usato ASV per ≥5 ore/notte, il punteggio ESS è diminuito da 9,0 al basale a 4,2 (p=0,028). L’uso dell’ASV durante lo studio è stato buono, con una media di 5 ore 20 minuti per notte a 3 mesi e 6 ore 22 minuti per notte a 6 mesi. L’ASV è stata anche ben tollerata e non sono stati riportati gravi effetti collaterali.
Quando non usare la servoventilazione adattiva
Come è sempre stato il caso, l’ASV non dovrebbe essere usata in qualsiasi situazione in cui è presente ipoventilazione allo stato basale. Pertanto, i gas sanguigni dovrebbero essere controllati prima dell’inizio del trattamento, come per qualsiasi altra strategia di ventilazione. Inoltre, sulla base dei risultati dello studio SERVE-HF, l’ASV è ora controindicata nei pazienti con HFrEF (EF ventricolare sinistro del 45% o meno) e CSA predominante. Tutti gli attuali destinatari dell’ASV che soddisfano questi criteri dovrebbero essere informati dei risultati del SERVE-HF e delle loro implicazioni e passare a un modo alternativo di terapia.
Monitoraggio della terapia
Al momento non ci sono linee guida pubblicate sul monitoraggio del paziente e sul follow-up durante la terapia ASV. Pertanto, i medici devono usare la loro esperienza nella pratica clinica e il buon senso. Prima di iniziare il trattamento, sembrerebbe appropriato controllare i sintomi di HF, rivedere attentamente l’anamnesi del paziente (prestando particolare attenzione agli eventi cardiaci) e, in caso di dubbio, determinare l’EF ventricolare sinistro utilizzando l’ecocardiografia (soprattutto nei pazienti che possono avere malattie cardiovascolari). Il follow-up a breve termine dovrebbe comprendere il controllo delle perdite, degli effetti collaterali e dell’aderenza alla terapia. La valutazione dell’efficacia del trattamento con la poligrafia o la PSG dopo 1-3 mesi, e un follow-up di 6 mesi che consiste in un’intervista clinica, lo scarico della macchina e una valutazione clinica completa sembra ragionevole. Il monitoraggio ecocardiografico continuo dell’EF sembra prudente quando ASV è usato in pazienti con malattia cardiaca.
Perspective and Future Directions
Un’importante area di ricerca in corso è quella di chiarire i meccanismi fisiopatologici alla base del segnale di sicurezza cardiovascolare identificato nei pazienti HFrEF trattati con ASV nello studio SERVE-HF. Questo permetterà di identificare sottogruppi specifici di pazienti HFrEF in cui ASV dovrebbe essere evitato, e altri che possono beneficiare della terapia ASV. I dati provenienti dal SERVE-HF major substudy5 e dall’analisi del trattamento, dallo studio ADVENT-HF (NCT01128816) e dai registri in corso, come lo studio di coorte prospettico multicentrico francese FACE,35 si spera forniranno alcune indicazioni sull’uso dell’ASV in sottogruppi di pazienti con HFrEF con CSA, pazienti con HFrEF e OSA o OSA con CSA coesistente e quelli con HFpEF ed entrambe le forme di SDB. Gli effetti dell’ASV nei pazienti con HF acuta scompensata sono in fase di studio nello studio CAT-HF (NCT01953874). Al di fuori dell’HF, sono necessari più dati sull’uso dell’ASV in pazienti con diversi fenotipi di CSA, comprese le apnee centrali indotte dal trattamento e dagli oppioidi.
Conclusione
Ci sono una serie di domande senza risposta sul posto attuale e futuro della terapia ASV in pazienti con varie forme di SDB. Sulla base dei risultati dello studio SERVE-HF, la terapia con ASV dovrebbe essere evitata nei pazienti con HFrEF e CSA predominante con CSR, e quando l’ASV è usato in altre indicazioni si raccomanda uno stretto monitoraggio del paziente, specialmente nei sottogruppi a rischio di sviluppare HF. Tuttavia, i dati attualmente disponibili suggeriscono che l’ASV ha effetti benefici nei pazienti con CSA emergente dal trattamento, apnee centrali associate a terapia oppioide a lungo termine senza ipoventilazione alveolare, RSI idiopatica, dopo ictus ischemico, e in quelli con HFpEF. I dati a lungo termine sugli effetti dell’ASV sulla morbilità e la mortalità in questi gruppi di pazienti non sono ancora disponibili e quindi l’inizio del trattamento è una decisione che dovrebbe essere presa individualmente per ogni paziente, e la terapia continua solo se il paziente mostra miglioramenti soggettivi e oggettivi durante il trattamento.
ADVENT-HF = The Effect of Adaptive Servo-Ventilation on Survival and Hospital Admissions in Heart Failure
CAT-HF = Cardiovascular Improvements with MV ASV Therapy in Heart Failure
FACE = French Cohort Study of Chronic Heart Failure Patients with Central Sleep Apnoea Eligible for Adaptive Servo-Ventilazione
SERVE-HF = Trattamento della respirazione disordinata nel sonno con predominanza di apnea notturna centrale mediante servoventilazione adattiva in pazienti con insufficienza cardiaca